Основные понятия гидропневмоавтоматики

Схема гидравлического привода с дроссельным регулированием
Основные свойства рабочих жидкостей и газов
Плотность – количество массы в единице объема: 
 График зависимости плотности воды от температуры График зависимости плотности воды от температуры |
 График зависимости изменения вязкости от температуры График зависимости изменения вязкости от температуры |
Вязкость
Свойство жидкости сопротивляться сдвигу или скольжению ее слоев.
 ,
, 
где:  – напряжение сдвига;
– напряжение сдвига;
 – динамический коэффициент вязкости;
– динамический коэффициент вязкости;
 – скорость течения жидкости;
– скорость течения жидкости;
 – расстояние между слоями жидкости.
– расстояние между слоями жидкости.
 – кинематический коэффициент вязкости
– кинематический коэффициент вязкости
Сжимаемость
Свойство жидкости изменять свой объем под действием давления.  ,
,
где:  – адиабатический модуль объемной упругости жидкости;
– адиабатический модуль объемной упругости жидкости;
 – объем рабочей жидкости;
– объем рабочей жидкости;
 – давление рабочей жидкости.
– давление рабочей жидкости.
Для газов:  или
или  – закон Бойля-Мариотта.
– закон Бойля-Мариотта.
Облитерация
Свойство жидкости заращивать (засорять) узкие каналы и капиллярные щели при ее течении под действием перепада давления.
Кавитация
Разрыв рабочей жидкости под действием высокого давления при наличии большого количества растворенного воздуха.
 Зависимость модуля объемной упругости АМГ-10 от давления и температуры Зависимость модуля объемной упругости АМГ-10 от давления и температуры |
 Зависимость объемного модуля упругости от содержания нерастворенного воздуха и давления Зависимость объемного модуля упругости от содержания нерастворенного воздуха и давления |
Для идеального газа
Зависимость давления и объема
Изотермный процесс – процесс, проходящий при постоянной температуре

Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Для студента самое главное не сдать экзамен, а вовремя вспомнить про него. 9745 –  | 7371 –
| 7371 –  или читать все.
или читать все.
91.146.8.87 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно
В каждой жидкости существует давление, обусловленное ее собственным весом. Так, например, давление на основание столба воды высотой 10 м составляет около 10 5 Па.
| h | высота столба жидкости, | Метр |
|---|---|---|
| p | давление в жидкости на глубине h, | Паскаль |
| g | ускорение свободного падения, | 9.81 м/c 2 |
| ρ | плотность жидкости, | кг/м 3 |
давление в жидкости равно ее весу, деленному на площадь,
Так как объем есть произведение высоты на площадь V = Sh, то
Плотность жидкости ρ зависит от температуры. Для очень точных вычислений плотность следует рассчитывать по специальной формуле. Давление на данной глубине одинаково во всех направлениях. Соотношение между единицами давления. Суммарное давление, обусловленное весом столба жидкости и давлением поршня, называют гидростатическим давлением.
Состояние идеального газа полностью описывается измеряемыми величинами: давлением, температурой, объемом. Отношение между этими тремя величинами определяется основным газовым законом:
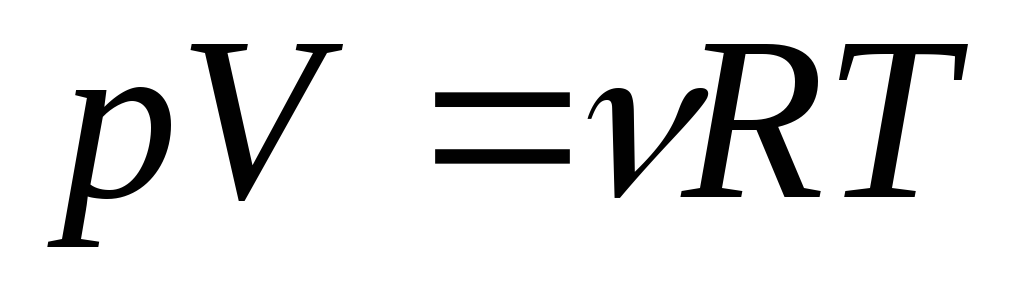 ,
,
где р – давление; V- объем; Т – температура;- количество идеального газа в молях;R- универсальная газовая постоянная (8,31 Дж/(Кмоль).
Если одна из величин давление, объем или температура остается постоянной, то другие две величины не могут быть изменены независимо друг от друга. Например, при постоянной температуре выполняется закон Бойля-Мариотта в виде:
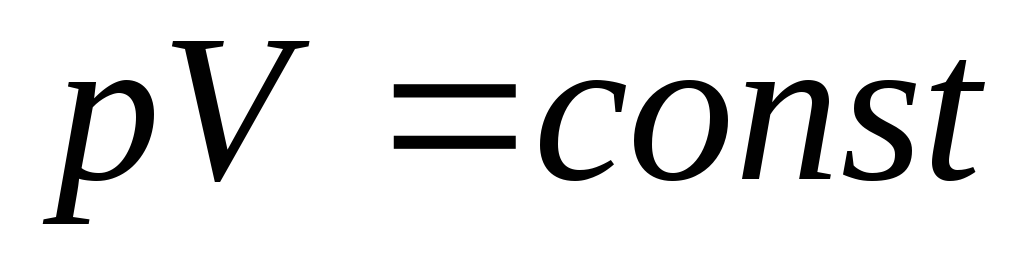
Проверка закона Бойля-Мариотта.
Измерение давления воздуха в шприце при изменении объема учитывая, что температура газа постояна.
Ручной вакуумный насос

Рис 1. Общий вид установки по изучению закона Бойля – Мариотта. (1) шприц, (2) манометр (отсчет производить по черной шкале), (3) ручной вакуумный насос
В данном эксперименте закон Бойля – Мариотта подтверждается с помощью установки показанной на рисунке 1. Объем воздуха в шприце определяется следующим образом:
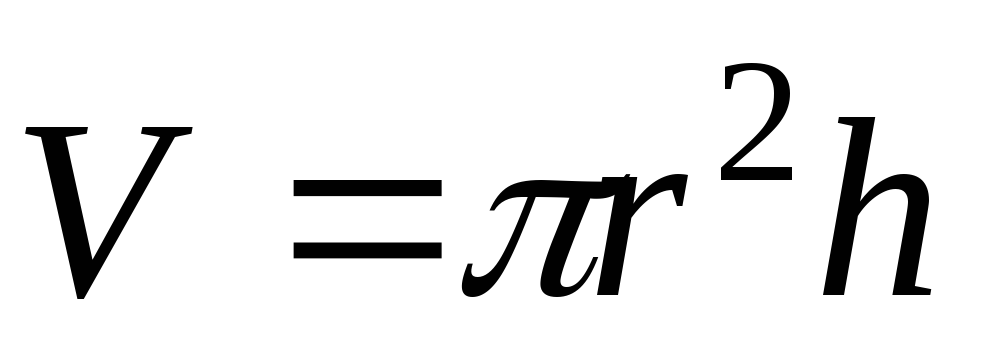
где rрадиус шприца, аh– расстояние от носика до поршня шприца.
Давление в системе нужно находить как:
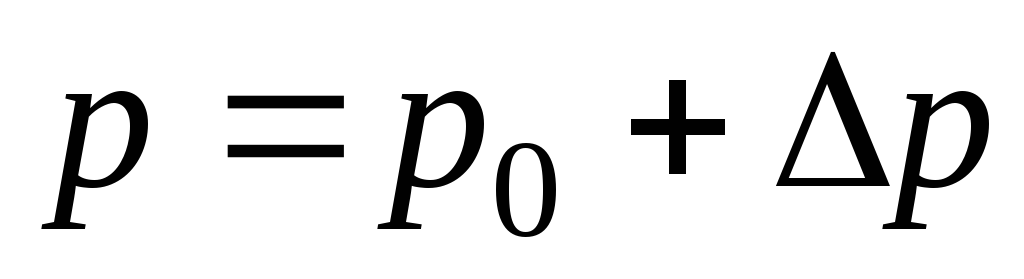
где pатмосферное давление, аp– давление, измеренное при помощи манометра.
Порядок выполнения работы
Установите поршень шприца на отметке 50 мл.
Плотно надеть свободный конец соединительного шланга ручного вакуумного насоса на выходной патрубок шприца.
Выдвигая поршень, увеличивайте объем с шагом 5 мл, фиксируйте показания маномета по черной шкале.
Чтобы определить давление под поршнем, надо из атмосферного давления вычесть показания монометра, выраженного в паскалях. Атмосферное давление равно приблизительно 1 бар, что соответствует 100 000 Па.
Для обработки результатов измерений следует учитывать наличие воздуха в соединительном шланге. Для этого измерьте расчитайте объем соединительного шланга, измерив длину шланга рулеткой, а диаметр шланга штангенциркулем, учитывая, что толщина стенок составляет 1,5 мм.
Постройте график измеренной зависимости объема воздуха от давления.
Рассчитайте зависимость объема от давления при постоянной температуре по закону Бойля-Мариотта и постройте график.
Сравните теоретические и экспериментальные зависимости.
2133. Зависимость давления газа от температуры при постоянном объеме (закон шарля)
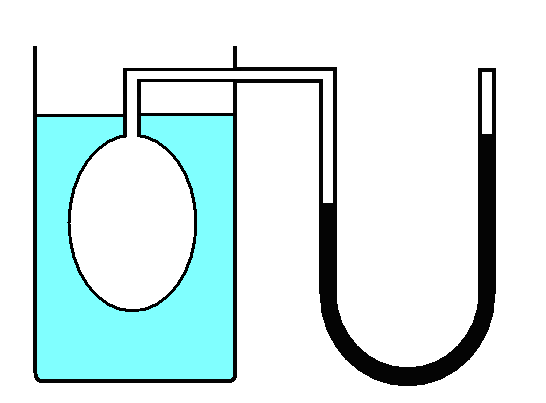
Рассмотрим зависимость давления газа от температуры при условии неизменного объема определенной массы газа. Эти исследования были впервые произведены в 1787 г. Жаком Александром Сезаром Шарлем (1746—1823). Газ нагревался в большой колбе, соединенной с ртутным манометром в виде узкой изогнутой трубки. Пренебрегая ничтожным увеличением объема колбы при нагревании и незначительным изменением объема при смещении ртути в узкой манометрической трубке. Таким образом, можно считать объем газа неизменным. Подогревая воду в сосуде, окружающем колбу, измеряли температуру газа по термометру Т, а соответствующее давлениер— по манометру. Наполнив сосуд тающим льдом, определяли давлениеро, и соответствующую температуруТо. Было установлено, что если при 0 С давлениеро, то при нагревании на 1 С приращение давления будет вро. Величинаимеет одно и то же значение (точнее, почти одно и тоже) для всех газов, а именно 1/273 C -1 . Величинуназывают температурным коэффициентом давления.
Закон Шарля позволяет рассчитать давление газа при любой температуре, если известно его давление при температуре 0 C. Пусть давление данной массы газа при 0 Cв данном объемеpo, а давление того же газа при температуреtp. Температура меняется наt, а давления изменяется нароt, тогда давлениерравно:
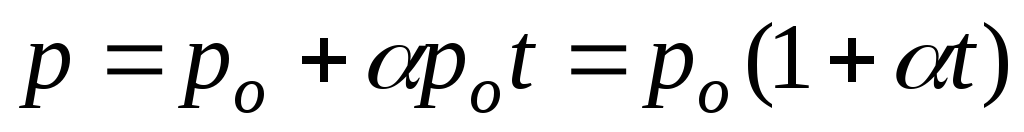
При очень низких температурах, когда газ приближается к состоянию сжижения, а также в случае сильно сжатых газов закон Шарля неприменим. Совпадение коэффициентов и, входящих в закон Шарля и закон Гей-Люссака, не случайно. Так как газы подчиняются закону Бойля — Мариотта при постоянной температуре, тоидолжны быть равны между собой.
Подставим значение температурного коэффициента давления в формулу температурной зависимости давления:

Величину (273+t) можно рассматривать как значение температуры, отсчитанное по новой температурной шкале, единица которой такая же, как и у шкалы Цельсия, а за нуль принята точка, лежащая на 273 ниже точки, принятой за нуль шкалы Цельсия, т. е. точки таяния льда. Нуль этой новой шкалы называют абсолютным нулем. Эту новую шкалу называют термодинамической шкалой температур, гдеTt+273 .
Тогда, при постоянном объеме справедлив закон Шарля:

Проверка закона Шарля
Определение зависимости давления газа от температуры при постоянном объеме
Определение абсолютной шкалы температур путем экстраполяции в сторону низких температур
Внимание: в работе используется стекло.
Будьте предельно аккуратны при работе с газовым термометром; стеклянным сосудом и мерным стаканом.
Будьте предельно внимательны при работе с горячей водой.
Мобильный CASSY Lab
Электрическая нагревательная плитка
Стеклянный мерный стакан
Ручной вакуумный насос
При откачке воздуха при комнатной температуре с помощью ручного насоса, создается давление на столб воздуха р0+р, где р – внешние давление. Капля ртути также оказывает давление на столб воздуха:
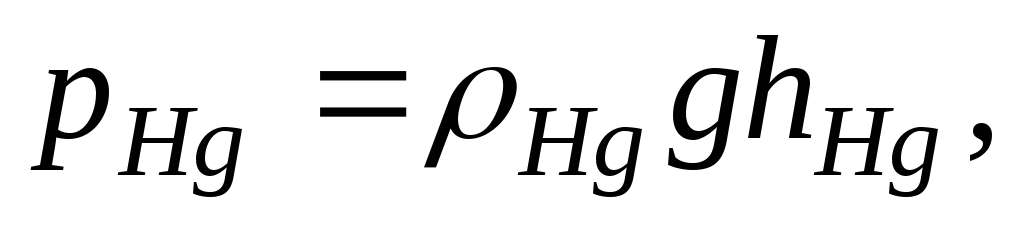
где Hg=13,6 г/см 3 – плотность ртути;g=9,81 м/c 2 – ускорение свободного падения; hHg – высота капли ртути.
Общее давление на столб воздухав газовом термометре определяется выражением:
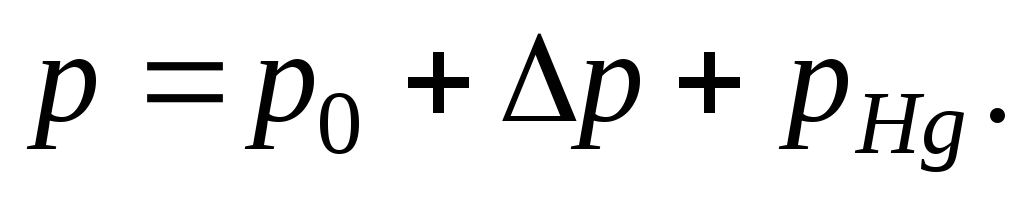
В данном эксперименте этот закон подтверждается с помощью газового термометра. Термометр помещают в воду с температурой около 90°С и эта система постепенно охлаждается. Откачивая воздух из газового термометра с помощью ручного вакуумного насоса, поддерживают постоянный объём воздуха во время охлаждения.
Порядок выполнения работы
Откройте заглушку газового термометра, подключите к термометру ручной вакуумный насос.
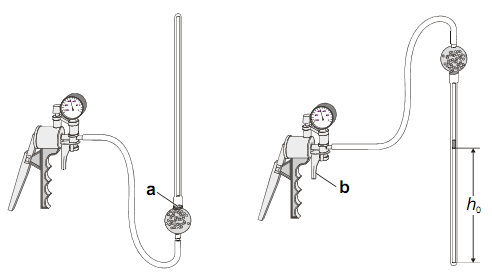
Поверните осторожно термометр как показано слева на рис. 2 и откачайте воздух из него с помощью насоса так, чтобы капелька ртути оказалась в точке a) (см. рис.2).
После того как капелька ртути собралась в точке a)поверните термометр отверстием наверх и спустите нагнетенный воздух ручкойb) на насосе (см. рис.2) осторожно, чтобы ртуть не разделилась на несколько капелек.
Нагреть воду в стеклянном сосуде на плитке до 90°С.
Налить горячую воду в стеклянный сосуд.
Поместить в сосуд газовый термометр, закрепив его на штативе.
Поместить термопару в воду, постепенно эта система охлаждается. Откачивая воздух из газового термометра с помощью ручного вакуумного наноса, поддерживаете постоянный объём столба воздуха в течении всего процесса охлаждения.
Фиксируйте показание манометра ри температуруТ.
Постройте зависимость полного давления газаp+p+pHgот температуры в о С.
Продолжите график до пересечения с осью абсцисс. Определите температуру пересечения, объясните полученные результаты.
По тангенсу угла наклона определите температурный коэффициент давления.
Рассчитайте зависимость давления от температуры при постоянном объеме по закону Шарля и постройте график. Сравните теоретические и экспериментальные зависимости.
 26-07-2019
26-07-2019 0 Просмотров
0 Просмотров 0 комментариев
0 комментариев 0 Рейтинг
0 Рейтинг