Осмос
Осмос– явление селективной диффузии определенного сорта частиц через полупроницаемую перегородку. Это явление впервые описал аббат Нолле в 1748 г. Перегородки, проницаемые только для воды или другого растворителя и непроницаемые для растворенных веществ, как низкомолекулярных, так и высокомолекулярных, могут быть изготовлены из полимерных пленок (коллодия) или гелеобразных осадков, например, ферроцианида меди Cu2[Fe(CN)6]; этот осадок образуется в порах перегородки стеклянного фильтра при погружении пористого материала сначала в раствор медного купороса (CuSO4 x 5H2O), а затем желтой кровяной соли K2[Fе(CN)6] . Вещества диффундируют через такую перегородку, что является важным случаем осмоса, позволяющим измерять осмотическое дав-ление, т. е. осмотическое давление– мера стремления растворенного вещества перейти вследствие теплового движения в процессе диффузии из раствора в чистый растворитель; распределяется равномерно по всему объему растворителя, понизив первоначальную концентрацию раствора.
За счет осмотического давления сила заставляет жидкость подниматься вверх, это осмотическое давление уравновешивается гидростатическим давлением. Когда скорости диффундирующих веществ станут равны, тогда осмос прекратится.
Закономерности:
1. При постоянной температуре осмотическое давление раствора прямо пропорционально концентрации растворенного вещества.
2. Осмотическое давление пропорционально абсолютной температуре.
В 1886 г. Я. Г. Вант-Гофф показал, что величина осмотического давления может быть выражена через состояние газа
Закон Авогадроприменим к разбавленным растворам: в равных объемах различных газов при одинаковой температуре и одинаковом осмотическом давлении содержится одинаковое число растворенных частиц. Растворы различных веществ, имеющие одинаковые молярные концентрации при одинаковой температуре, имеют одинаковое осмотическое давление. Такие растворы называются изотоническими.
Осмотическое давление не зависит от природы растворяемых веществ, а зависит от концентрации. Если объем заменить на концентрацию, получим:
Рассмотрим закон Вант-Гоффа: осмотическое давление раствора численно равно тому давлению, которое производило бы данное количество растворенного вещества, если бы оно в виде идеального газа занимало при данной температуре объем, равный объему раствора.
Все описанные законы относятся к бесконечно разбавленным растворам.
Парциальное давление– то давление, которое оказывал бы газ, входящий в газовую смесь, если бы из нее были удалены все остальные газы при условии сохранения постоянными температуры и объема.
Общее давление газовой смеси определяется законом Дальтона: общее давление смеси газов, занимающих определенных объем, равно сумме парциальных давлений, которыми обладал бы каждый отдельно взятый газ, если бы он занимал объем, равный объему смеси газов.
где Р – общее давление;
Рк – парциальное давление компонентов.
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Сдача сессии и защита диплома – страшная бессонница, которая потом кажется страшным сном. 8546 –  | 7049 –
| 7049 –  или читать все.
или читать все.
91.146.8.87 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно
Газовая смесь находится в состоянии равновесия, если концентрации компонентов и её параметры состояния во всём объёме имеют одинаковые значения. При этом температура всех газов, входящих в смесь, одинакова и равна температуре смеси Тсм.
В равновесном состоянии молекулы каждого газа рассеяны равномерно по всему объёму смеси, то есть имеют свою определённую концентрацию и, следовательно, своё давление рi, Па, которое называется парциальным. Оно определяется следующим образом.
Парциальное давление равно давлению данного компонента при условии, что он один занимает весь объём, предназначенный для смеси при температуре смеси Тсм.
По закону английского химика и физика Дальтона, сформулированному в 1801 году, давление смеси идеальных газов рсм равно сумме парциальных давлений её компонентов рi:
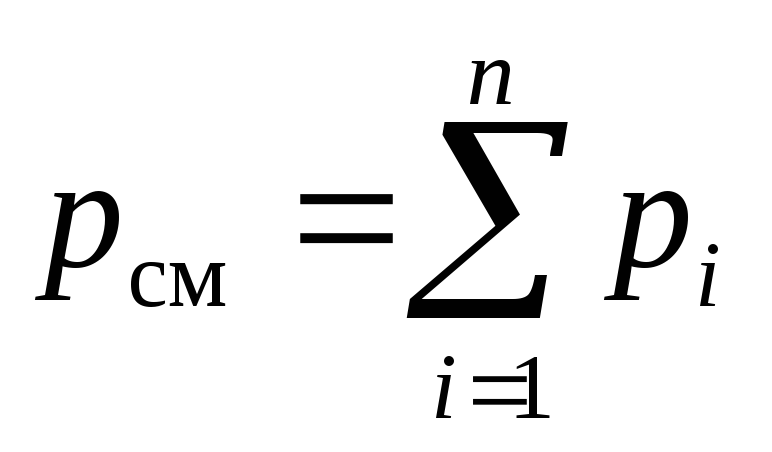 , (2)
, (2)
где n – число компонентов.
Выражение (2) также называется законом парциальных давлений.
3.3. Приведённый объём компонента газовой смеси. Закон Амага
По определению приведённым объёмом i-го компонента газовой смеси Vi, м 3 , называется объём, который один этот компонент мог бы занимать при условии, что его давление и температура будут равны давлению и температуре всей газовой смеси.
Закон французского физика Амага, сформулированный примерно в 1870 году, гласит: сумма приведённых объёмов всех компонентов смеси равна объёму смеси Vсм:
 , м 3 . (3)
, м 3 . (3)
3.4. Химический состав газовой смеси
Химический состав газовой смеси может задаваться тремя различными способами.
Рассмотрим газовую смесь, состоящую из n компонентов. Смесь занимает объём Vсм, м 3 , имеет массу Мсм, кг, давление рсм, Па и температуру Тсм, К. Также число молей смеси равно Nсм, моль. При этом масса одного i-го компонента mi, кг, а число молей этого компонента νi, моль.
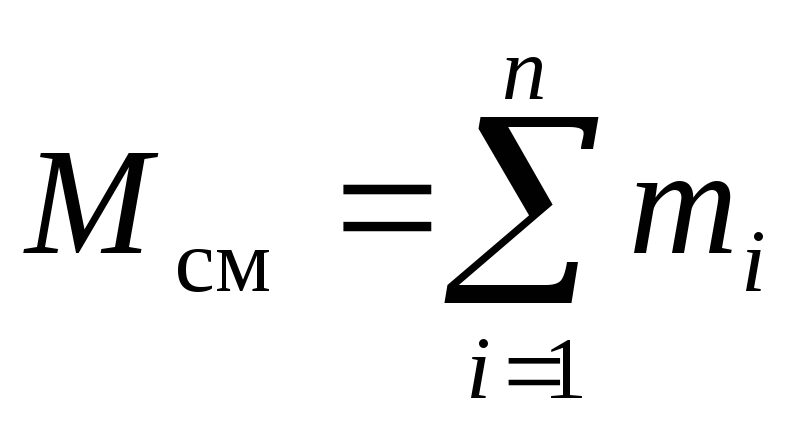 , (4)
, (4)
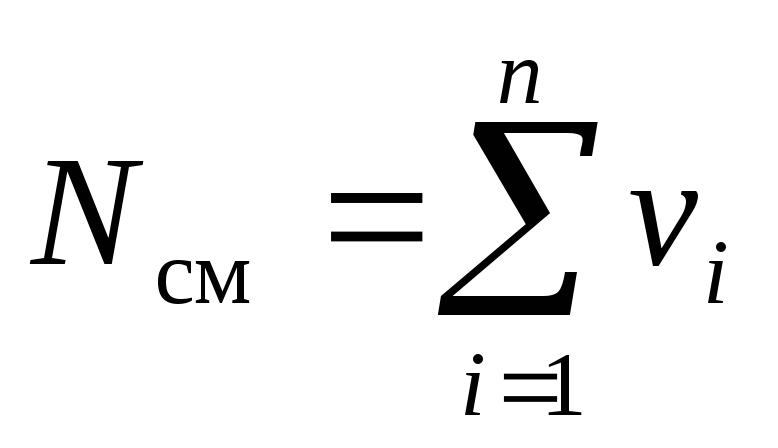 . (5)
. (5)
Используя для рассматриваемой смеси закон Дальтона (2) и Амага (3) можно записать:
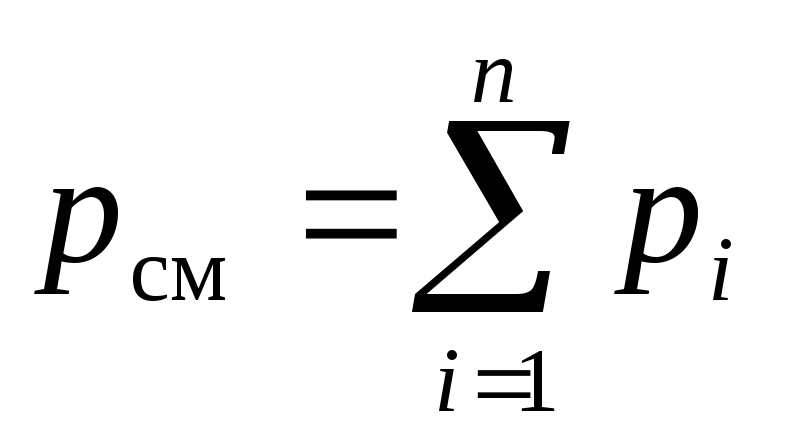 , (6)
, (6)
 , (7)
, (7)
где рi – парциальное давление i-го компонента, Па; Vi – приведённый объём i-го компонента, м 3 .
Однозначно химический состав газовой смеси может быть задан либо массовыми, либо мольными, либо объёмными долями её компонентов:
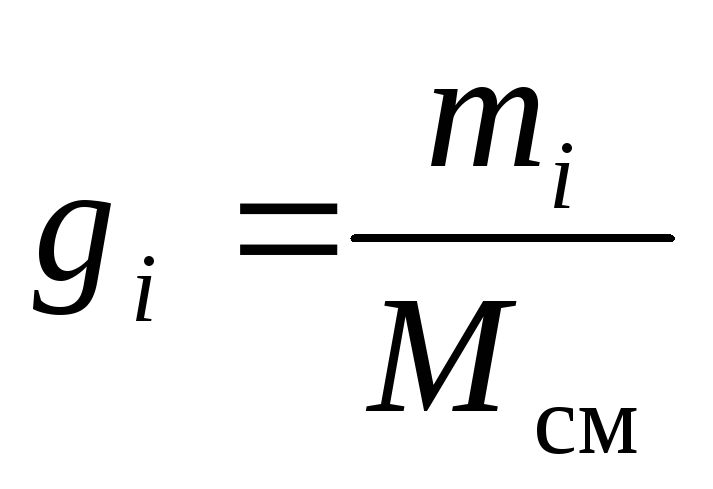 , (8)
, (8)
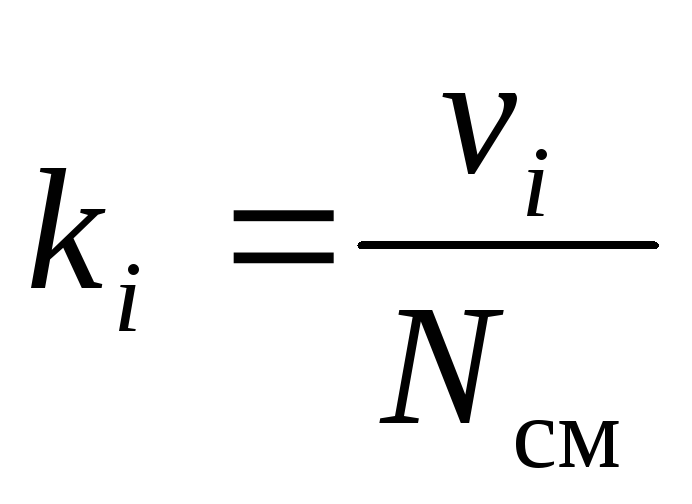 , (9)
, (9)
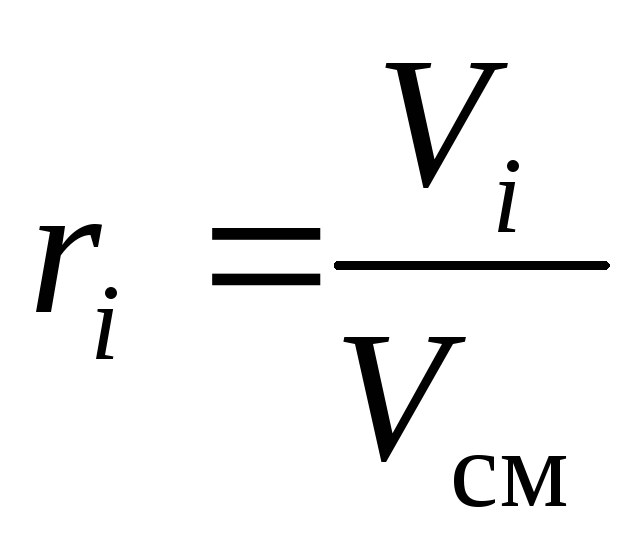 , (10)
, (10)
где gi, ki и ri – массовая, мольная и объёмная доли i-го компонента смеси соответственно (безразмерные величины).
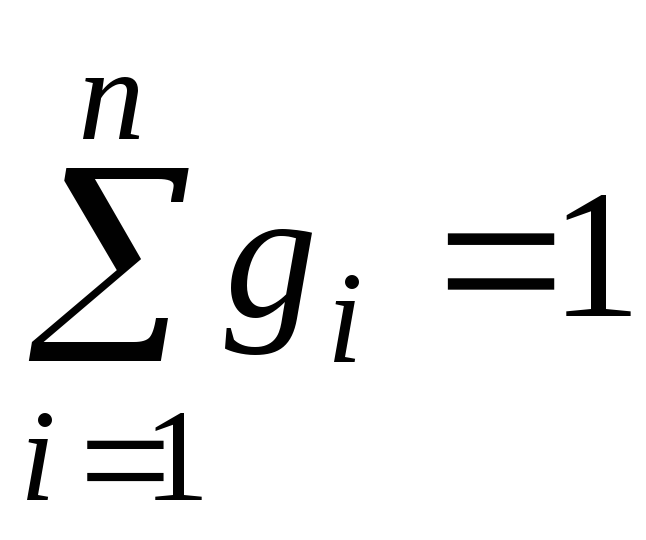 ,
, 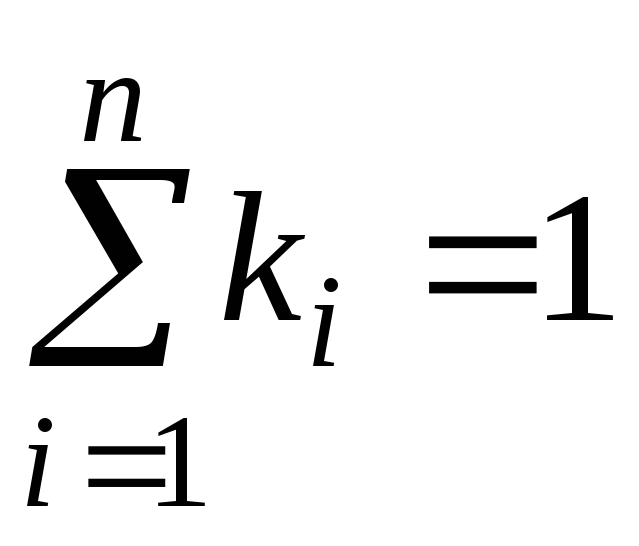 ,
,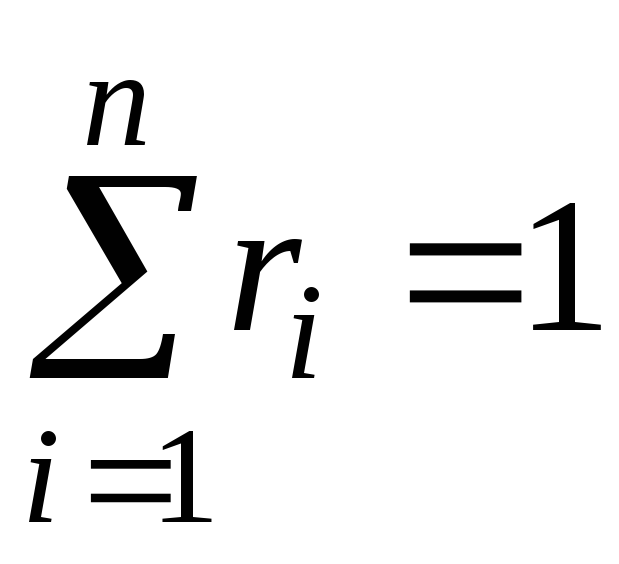 . (11)
. (11)
Часто на практике химический состав смеси задаётся не долями i-го компонента, а его процентами.
Например, в теплотехнике приближённо принимается, что сухой воздух состоит из 79 объёмных процентов азота и 21 объёмного процента кислорода.
Процент i-го компонента в смеси вычисляется путём умножения его доли на 100.
Для примера с сухим воздухом будем иметь:
 ,
, 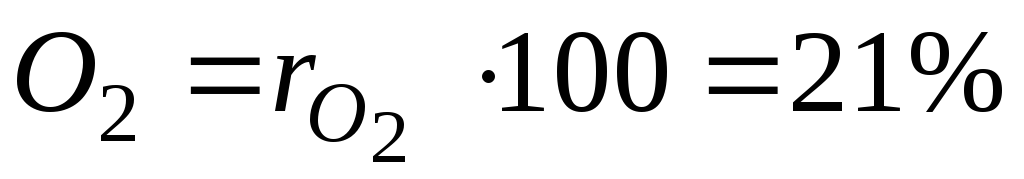 . (12)
. (12)
где 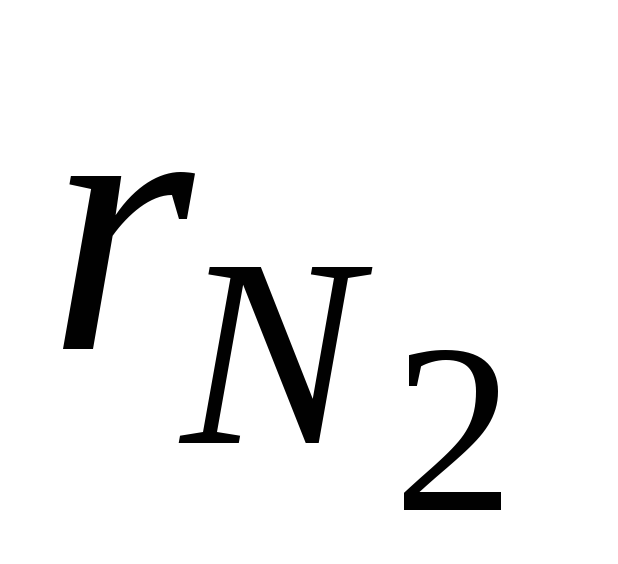 и
и 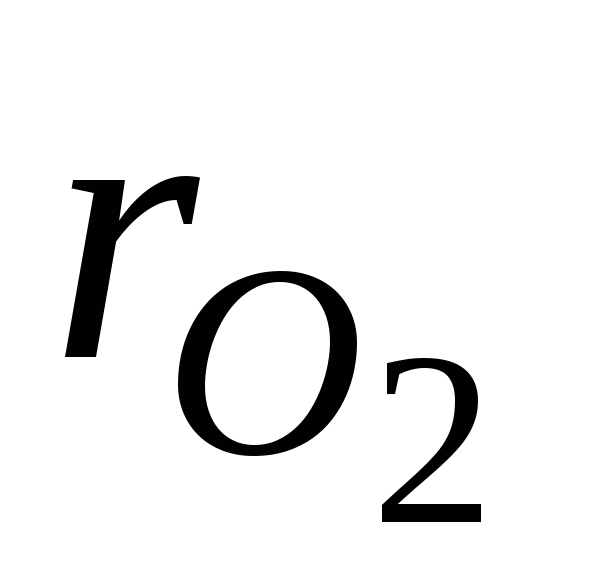 – объёмные доли азота и кислорода в сухом воздухе; N2 и О2 – обозначение объёмных процентов азота и кислорода соответственно, % (об.).
– объёмные доли азота и кислорода в сухом воздухе; N2 и О2 – обозначение объёмных процентов азота и кислорода соответственно, % (об.).
1) Мольные доли идеальной смеси численно равны объёмным долям: ki = ri. Докажем это.
Пользуясь определением объёмной доли (10) и законом Амага (3) можем записать:
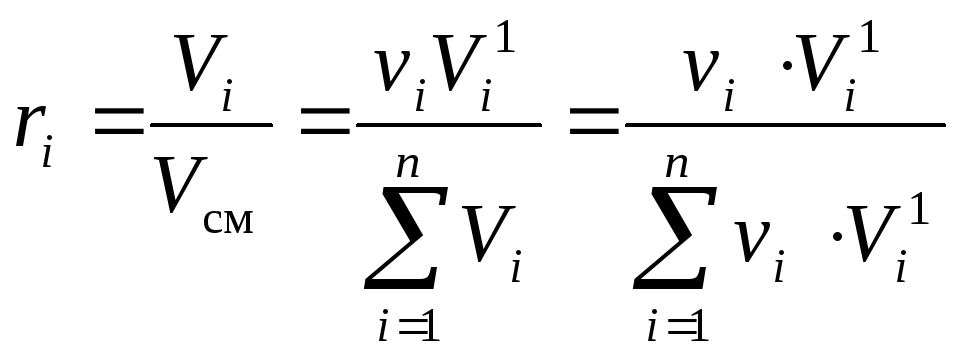 , (13)
, (13)
где Vi – приведённый объём i-го компонента, м 3 ; νi – число молей i-го компонента, моль;  – объём одного моля i-го компонента при давлении смеси рсм и температуре смеси Тсм, м 3 /моль.
– объём одного моля i-го компонента при давлении смеси рсм и температуре смеси Тсм, м 3 /моль.
Из закона Авогадро (см. п. 2.3 данного приложения) следует, что при одинаковых температуре и давлении один моль любого газа (компонента смеси) занимает один и тот же объём. В частности, при Тсм и рсм это будет некоторый объём V 1 , м 3 .
Сказанное позволяет записать равенство:
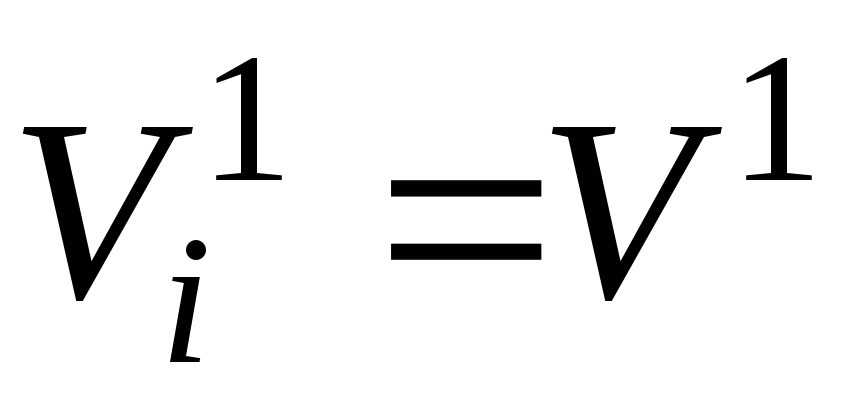 . (14)
. (14)
Подставляя (14) в (13) получаем требуемое:
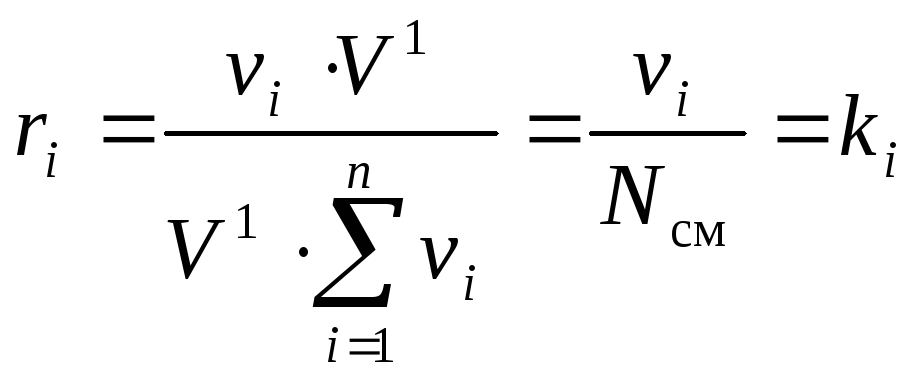 . (15)
. (15)
2) Объёмные доли компонентов газовой смеси можно рассчитать, зная их парциальные давления. Покажем это.
Рассмотрим i-ый компонент идеальной газовой смеси в двух различных состояниях: когда он находится при своём парциальном давлении рi; когда он занимает свой приведённый объём Vi.
Уравнение состояния идеального газа справедливо для любых его состояний, в частности, и для двух, названных выше.
В соответствии с этим, и учитывая определение удельного объёма, можем записать:
 , (16)
, (16)
 ,(17)
,(17)
После деления обоих частей (16) и (17) друг на друга получаем требуемое:
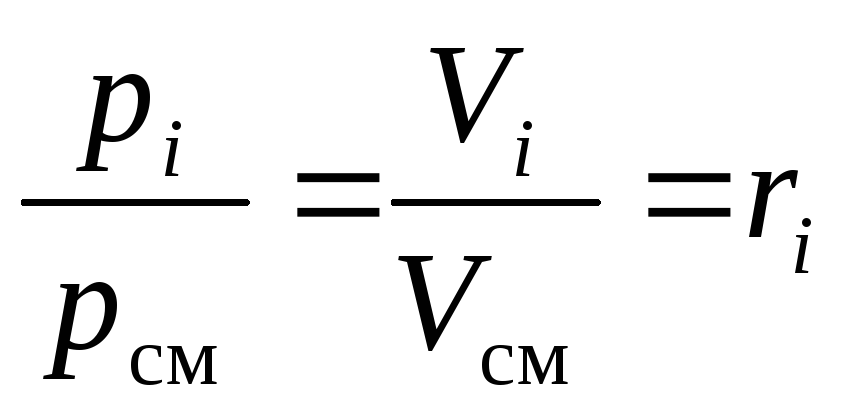 . (18)
. (18)
Из (18) видно, что парциальные давления компонентов смеси можно рассчитать по её химическому составу, при известном общем давлении смеси рсм:
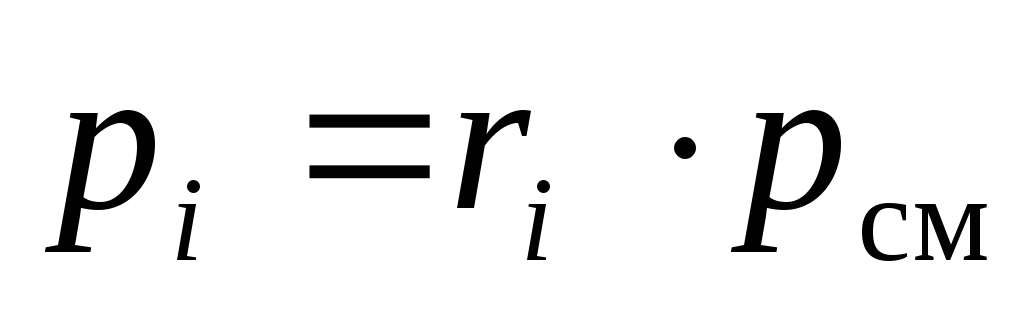 . (19)
. (19)
Парциа́льное давление (лат. partialis «частичный» от pars «часть») — давление отдельно взятого компонента газовой смеси [1] [2] . Общее давление газовой смеси является суммой парциальных давлений её компонентов.
В химии парциальное давление газа в смеси газов определяется как указано выше. Парциальное давление газа, растворённого в жидкости, является парциальным давлением того газа, который образовался бы в фазе газообразования в состоянии равновесия с жидкостью при той же температуре. Парциальное давление газа измеряется как термодинамическая активность молекул газа. Газы всегда будут вытекать из области с высоким парциальным давлением в область с более низким давлением; и чем больше разница, тем быстрее будет поток. Газы растворяются, диффундируют и реагируют соответственно их парциальному давлению и не обязательно зависимы от концентрации в газовой смеси.
Содержание
Законы Дальтона парциального давления [ править | править код ]
Для идеального газа парциальное давление в смеси равно давлению, которое будет оказываться, если бы он занимал тот же объём, что и вся смесь газов, при той же температуре. Причина этого в том, что между молекулами идеального газа по определению не действуют силы притяжения или отталкивания, их соударения между собой и со стенками сосуда абсолютно упруги, а время взаимодействия между молекулами пренебрежимо мало по сравнению со средним временем между столкновениями. Насколько условия реально существующей смеси газов близки этому идеалу, настолько общее давление смеси равно сумме парциальных давлений каждого газа смеси, как это формулирует закон Дальтона [3] . Например, дана смесь идеального газа из азота (N2), водорода (H2) и аммиака (NH3):
P = P N 2 + P H 2 + P N H 3 <\displaystyle P=P_<<\mathrm 
P N 2 <\displaystyle P_<<\mathrm 
P H 2 <\displaystyle P_<<\mathrm 
P N H 3 <\displaystyle P_<<\mathrm 
Смеси идеальных газов [ править | править код ]
Мольная доля отдельных компонентов газа в идеальной газовой смеси может быть выражена в пределах парциальных давлений компонентов или молей компонентов:
x i = P i P = n i n <\displaystyle x_<\mathrm >= <\frac >>
>= <\frac >>
и парциальное давление отдельных компонентов газов в идеальном газе может быть получено используя следующее выражение:
P i = x i ⋅ P <\displaystyle P_<\mathrm >=x_ <\mathrm >\cdot P> 
Мольная доля отдельного компонента в газовой смеси равна объёмной доле этого компонента в газовой смеси [4] .
 26-07-2019
26-07-2019 0 Просмотров
0 Просмотров 0 комментариев
0 комментариев 0 Рейтинг
0 Рейтинг