Адекватное и быстрое обезболивание при инфаркте миокарда (первоочередная проблема) должно проводиться еще на догоспитальном этапе. Оно помогает разорвать порочный круг (ишемия миокарда -> боль -> ишемия миокарда), снизить активность симпатической нервной системы (уменьшить работу миокарда), ослабить рефлекторные влияния из очага поражения на тонус периферических сосудов и сердечный выброс (предотвратить формирование рефлекторного КШ).
Подход к купированию боли состоит из двух этапов: уменьшения ишемии миокарда и непосредственного влияния на боль. Антиишемическая терапия включает реинфузию, назначение р-АБ, нитратов, ингаляции кислорода.
Больному нельзя давать половинные дозы анальгетиков, он не должен терпеть боль – это угроза его жизни. Важный аспект обезболивания — снижение ПО2 миокардом (на фоне строгого постельного режима, нормализации ЧСС и АД). Оптимальный путь обезболивания — устранение причины боли, т.е. восстановление коронарного кровотока (тромболизис).
Для купирования боли в отсутствие гипотонии сразу используют не более 3 раз сублингвальный прием нитроглицерина (в домашних условиях, если нет возможности ввести парентерально обезболивающие), потом его назначают внутривенно капельно. Если боль не купируется, то обычно вводят внутривенно наркотические ЛС (но не внутримышечно или подкожно, ибо в этом случае анальгезирующий эффект слаб и наступает поздно). При болевом синдроме на фоне возбуждения и повышения АД наркотические ЛС назначают сразу. Они уменьшают ишемию миокарда, страх и тахикардию. Наркотики купируют боль не только прямо, но и опосредованно за счет снижения тонуса САС, что уменьшает П02 миокардом. В качестве дополнительных мер (когда внутривенное введение опиатов оказалось недостаточно эффективным) назначают внутривенно АБ и нитраты.
Купирование боли при инфаркте миокарда включает следующее.
• Прием таблетки нитроглицерина под язык, если нет гипотонии (ибо даже малая его доза может вызвать гипотонию, что опасно для больного, особенно на фоне брадикардии), повторить через 5—10 мин (если больной находится дома). Сублингвальный прием нитроглицерина очень редко «открывает» окклюзивную коронарную артерию. Следует узнать у больного, не принимал ли он последнее время силденафил (виагру), так как прием нитроглицерина на этом фоне в последние 24 ч может вызвать опасное падение АД. Если он неэффективен, то в больнице вводят наркотические ЛС. У части больных ИМ анальгетики только временно устраняют болевой синдром. В этих случаях внутривенно капельно вводят 100 мл 1% раствора нитроглицерина с начальной скоростью 5-10 мкг/мин и постепенным увеличением скорости до 20 мкг/мин и более (на 5— 10 мкг/мин каждые 5-10 мин) под контролем АД (лучше проводить непрерывную инфузию в течение 48-72 ч) и ЯСС (может повышаться более чем на 10 уд/мин, но не должно превышать 110 уд/мин).
САД должно не снижаться менее 100 мм рт. ст. или уменьшаться на 15% от исходного у больных с нормальным АД (на 30% у гипертоников). Нитроглицерин полезен в лечении ИМ, осложненного ОСН в случае сохранения симптоматики или повышения АД. Вместо нитроглицерина можно использовать изокет (внутривенно капельно 50 мг в 100 мл изотонического раствора со скоростью вливания 8—10 капель в минуту под контролем АД). Нитраты не назначают больным с САД менее 90 мм рт. ст., ЧСС менее 50 уд/мин или более 110 уд/мин и подозрением на ИМ ПЖ. После внутривенного введения нитратов больным с СН или сохраняющейся ишемией назначают их орально с большими временными интервалами, чтобы избежать тахифилаксии. Нитраты нормализуют коронарный кровоток, особенно в ишемизированной зоне, и уменьшают боль (за счет снижения ПО2 миокардом вследствие возникновения периферической вазодилатаиии), зону некроза, напряжение и объем желудочков, ремоделирование миокарда в пораженной зоне и частоту механических осложнений. Но надо иметь в виду, что нитраты купируют ангинозную боль, тогда как при ИМ превалирует боль от околонекрозных участков, поэтому здесь лучше использовать наркотические ЛС.
• Назначение оксигенотерапии (100% увлажненный кислород) позволяет повысить диффузию кислорода в ишемизированный миокард. Она должна проводиться каждому больному через носовой катетер в первые 6 ч, а при появлении признаков застоя в легких, ОЛ или КШ — через маску или интубационную трубку.
• АБ показаны всем больным (при отсутствии противопоказаний) в первые 4—12 ч инфаркта миокарда независимо от проведения тромболизиса при гипердинамических состояниях (тахиаритмиях, повышении АД), повторно возникающих ангинозных приступах, не «отпускающих» после введения наркотических ЛС, прогрессирующем росте кардиоспецифических ферментов (что указывает на расширение зоны ИМ). Р-АБ снижают симпатическое влияние на миокард, ЧСС и ПО2 миокардом (этим сохраняют его жизнеспособность), вероятность повторной ишемии (и нового ИМ), зону некроза миокарда (при раннем назначении), боль, потребность в анальгетиках и появление опасных аритмий. Для быстрого эффекта Р-АБ назначают сначала в малой дозе внутривенно болюсом метопролол по 5 мг через каждые 5—10 мин, 3 болюса — под контролем ЭКГ и АД (ориентиры — целевая ЧСС 50—60 уд/мин, САД 100 мм рт. ст. и более) и потом внутрь (обычно при сохранении стабильной гемодинамики после 3-й дозы) по 50 мг через каждые 6 ч в течение 2 дней, а позднее – по 100 мг 2 раза в сутки; альтернатива — внутрь пропранолол (по 50 мг через каждые 6 ч; поддерживающая доза — 50—200 мг/сут) или атенолол (внутривенно 2 болюса по 5 мг с интервалом в 5 мин, потом поддерживающая доза — 100 мг/сут).
У больных с пограничными параметрами гемодинамики лечение начинают с небольших доз АБ (метопролол 12,5—25 мг 2 раза в сутки). Орально АБ должны использоваться в лечении ИМ как можно раньше, независимо от параллельного проведения ПЧКА или тромболизиса. Р-АБ должны назначаться в период клинических проявлений ИМ до тех пор, пока не появятся «специфические» осложнения (слабость ЛЖ, брадикардия). Эти ЛС уменьшают ударный объем сердца, который при ИМ уже заметно снижен. Они противопоказаны при ОСН (влажные хрипы выше 10 см над диафрагмой); тяжелой ХСН с малой ФВЛЖ; гипотонии (САД менее 90 мм рт. ст.); брадикардии (ЧСС менее 60 уд/мин); прогрессирующей АВ-блокаде II степени (или PQ более 0,24 с); бронхоспастическом синдроме (даже в анамнезе); выраженной патологии периферических артерий, инсулинзависимом СД. Следует избегать назначения АБ у больных с неясной тахикардией, так как это может вызвать декомпенсацию имеющейся СН у больных с компенсаторной тахикардией.
В ПОМОЩЬ ПРАКТИЧЕСКОМУ ВРАЧУ Провоторов В.М., Барташевич Б.И., Усков В.М.
Воронежская государственная медицинская академия им. Н.Н. Бурденко
Проблема обезболивания – одна из важнейших при лечении инфаркта миокарда (ИМ). Конечный результат интенсивной терапии во многом зависит от эффективности аналгезии [3, 4, 29, 47]. Чем выраженное и продолжительнее болевой синдром, тем больше опасность развития тяжелых осложнений [1, 2, 21, 42, 44]. Главной задачей обезболивания является смягчение стрессорной реакции при минимальном угнетающем действии медикаментов на системы кровообращения и дыхания [19, 20, 49]. Снижение или полное купирование болевого стресса способствуют уменьшению числа осложнений и более благоприятному течению заболевания [22, 54]. В настоящее время для купирования болевого синдрома у больных ИМ используется большое количество лекарственных средств с различными механизмами действия [48].
Наркотические аналгетики (НА)
Аналгетики – это лекарственные средства, обладающие специфической особенностью ослаблять или устранять чувство боли [56]. Среди них наиболее мощными по действию являются НА.
Морфин гидрохлорид является основным представителем группы НА. Используется внутривенно в дозе 3-5 мг, внутримышечно или подкожно – 10-20 мг. Наибольший обезболивающий эффект развивается в зависимости от способа введения через 30-60 минут. Полного обезболивания обычно удается достичь в 15-30% случаев, неполного – в 40-60%. В настоящее время морфин реже используется для обезболивания больных ИМ ввиду возможности развития негативных эффектов (угнетение дыхательного центра, тошнота, рвота, парез желудочно-кишечного тракта, задержка мочеиспускания и т.п.) [45].
Другим НА, часто используемым для обезболивания ИМ, является промедол [20]. Препарат по своим свойствам близок к морфину, но меньше угнетает дыхательный центр, меньше возбуждает рвотный центр и центр блуждающего нерва. Разовая доза при внутривенном и внутримышечном введении у больных ИМ составляет 10-20 мг.
Наиболее популярным НА является фентанил [50]. Это синтетический НА, с выраженным аналгетическим действием (в 100 раз превосходит морфин). При внутривенном введении препарата в дозе 0,05-0,1 мг (1-2 мл 0,005% раствора) эффект наступает через 1-3 минуты и продолжается в течение 15-30 минут [45]. Характеризуется коротким периодом действия (около 30 минут). При внутривенном введении в дозе 0,1-0,5 мг может вызвать резкое угнетение дыхания, ригидность грудной клетки, брадикардию.
В последние годы для обезболивания ИМ все чаще используются пентазоцин, нубаин, трамал [21, 31]. Пентазоцин (фортрал) является слабым антагонистом опиатов. Способен снимать угнетающее действие на дыхание фентанила, сохраняя аналгезию. Длительность аналгезии при введении препарата в дозе 30 мг в среднем составляет 3-4 часа. Нубаин является аналгетиком синтетическою ряда. Обезболивающий эффект после внутривенного введения 10-20 мг наступает через 3-5 минут, после внутримышечного – через 5-10 минут. Длительность эффекта – 4-6 часов. Препарат вводится, в среднем, 3-4 раза в сутки [32]. Хорошие результаты обезболивания ИМ отмечаются при использовании трамадола в средней дозе 1,4 мг/кг (достигнуто достаточное обезболивание в 58,8% случаев) [31]. Препарат более безопасен по сравнению с морфином и промедолом, поэтому его более целесообразно использовать у больных пожилого возраста с умеренным болевым синдромом или с сердечной недостаточностью.
Внутривенные и внутримышечные инъекции НА и их аналогов, как правило, малоэффективны при разрывах сердечной мышцы и затяжном течении инфаркта миокарда [5, 47]. Морфин, промедол в небольших дозах вызывают угнетение спастических рефлекторных реакций коронарных сосудов, тогда как при применении больших доз этих препаратов проявляется противоположный эффект – повышение тонуса и спастические реакции венечных сосудов [37]. Кроме того, наркотические аналгетики в больших дозировках оказывают выраженный отрицательный инотропный эффект, вызывают снижение артериального давления и брадикардию [56].
При возникновении депрессии дыхания вследствие использования НА, необходимо 1 мл налоксона (0,04 мг) развести в 9 мл изотонического раствора и ввести внутривенно. При отсутствии эффекта следует повторно вводить препарат в той же дозировке каждые 1-2 минуты до восстановления и нормализации дыхания [31]. Следует помнить, что использование с целью снижения дыхательной депрессии аналептиков, увеличивает потребность нервных клеток в кислороде и ведет к гипоксии. Применение специфических антидотов типа налорфина снимает не только депрессию дыхания, но и аналгезию [20, 56].
Нейролептаналгезия (НЛА)
При купировании болевого синдрома у больных ИМ необходимо блокировать не только центральные, но и клеточные, эндокринные и вегетативные реакции организма на повреждающие воздействия [29, 33]. Эта задача может быть решена с помощью НЛА – сочетанного применения аналгетика и нейролептика. НЛА оказывает селективное воздействие на клетки зрительного бугра, подбугорной области, ретикулярную формацию, вызывая потерю болевой чувствительности, состояние психического и двигательного покоя без наступления сна. В качестве нейролептика обычно используется дроперидол [45]. Препарат вызывает выраженное нейровегетативное торможение, оказывает противошоковый эффект, обладает противорвотным действием [34], Аналгетическим компонентом чаще всего служит фентанил, но может использоваться другой препарат (трамал, ненаркотические аналгетики). Существует готовая смесь – таламонал, которая содержит 0,05 мг фентанила и 2,5 мг дроперидола в 1 мл. Обезболивающий эффект НЛА можно усилить предварительным введением 10-15 тыс. ЕД гепарина [22].
НЛА обеспечивает хорошее обезболивание у большинства больных. У больных пожилого и старческого возраста с выраженной сопутствующей соматической патологией при использовании классической НЛА выявляются нарушения функции внешнего дыхания [23, 26]. Чтобы при проведении НЛА избежать угнетения дыхания, целесообразно усиливать ненаркотический компонент (анальгин, баралгин, трамал и т.п.) [22, 43, 50].
Атаролгезия
Атаралгезией называют метод комбинированного использования транквилизаторов и НА (например, 2 мл 0,005% раствора фентанила и 2 мл 0,5% раствора седуксена) [44]. Клиника атаралгезии сходна с клиникой нейролептаналгезии, но характеризуется меньшими нарушениями дыхания и гемодинамики, что позволяет широко использовать данную методику у больных пожилого и старческого возраста с выраженной сопутствующей патологией [43]. Наибольшее применение для атаралгезии из транквилизаторов получил седуксен (диазепам, реланиум) [31, 37, 41]. Препарат не оказывает прямого влияния на миокард, но кратковременно уменьшает общее периферическое сопротивление, благодаря чему может несколько снижаться артериальное давление и сердечный выброс. Препарат параллельно с торможением поведенческих проявлений ноцицептивных реакций значительно уменьшает прессорные реакции артериального давления и тахикардию, усиливает кардиохронотропный эффект барорефлекса и модулирующую функцию "аналгетических" систем среднего мозга. В качестве аналгетика чаще всего используются фентанил, промедол, пентазоцин в обычных или несколько уменьшенных дозировках (возможно использование других препаратов) [28, 31].
Клофелин
Клофелин (клонидин) – водорастворимый препарат, легко проникающий через гематоэнцефалический барьер. Обладает селективными альфа-2-адреностимулирующими свойствами. Имеющиеся данные позволяют рекомендовать препарат для включения в комплекс аналгетических средств, используемых при болевом синдроме у больных с инфарктом миокарда [28]. Помимо обезболивающего эффекта клофелин способен обеспечивать уменьшение работы поврежденного миокарда путем уменьшения адренергических воздействий на сердце. Использование препарата показано у больных с артериальной гипер- и нормотензией. Его применение ограничено при наличии артериальной гипотензии. По мнению В.А. Михайловича и соавт. [28], клофелин, обладающий одновременно аналгетическим и гемодинамическим свойствами, может занять промежуточную позицию между собственно аналгетическими препаратами и специфическими способами лечения ИМ, в основе действия которых лежит уменьшение нагрузки на миокард.
Средства для ингаляционного наркоза
Наиболее широко для обезболивания у больных ИМ используется закись азота [45]. Аналгезирующее действие закиси наступает при концентрации 35-45 об.%. Утрата сознания наблюдается при концентрации, равной 60-80%, но не у всех пациентов. Закись азота обладает достаточным аналгетическим эффектом при купировании болевого синдрома у большинства пациентов с ИМ. В концентрациях до 80% она практически безвредна для организма. Использование более высоких концентраций ведет к развитию гипоксии. Хотя закись азота принято считать одним из традиционных способов обезболивания при ИМ, в настоящее время имеется ряд публикаций, заставляющих более осторожно подходить к ее использованию. Выявлено, что закись азота способна вызывать сужение эпикардиальных коронарных артерий и усугублять повреждение сердечной мышцы с последующим уменьшением насосной функции сердца [15, 60].
Другие средства для ингаляционного наркоза (пентран, трилен и др.) в настоящее время используются редко для проведения обезболивания у больных ИМ или применяются по определенным показаниям (необходимость выключения сознания при кардиоверсии, выполнение болезненных манипуляций, проведение искусственной вентиляции легких и т.п.) [37]. Это обусловлено необходимостью использования специальной наркозной аппаратуры и специфическими особенностями препаратов (способность сенсибилизации миокарда и т.п.) [28].
Электрообезболивание
Транскраниальная электроаналгезия представляет собой воздействие электрическим током на структуры головного мозга, которое способно вызывать состояние обезболивания или снижать интенсивность болевых ощущений [30]. Механизм возникновения аналгезии при электростимуляционных способах обезболивания связан с активацией эндогенных опиатных структур. Это приводит к высвобождению опиоидных пептидов, в частности, бета-эндорфина, концентрация которого в плазме и спинномозговой жидкости возрастает в несколько раз. Кроме того, стимуляция толстых периферических афферентных волокон угнетает интернейроны головного мозга и не позволяет болевым импульсам, проводящимся по тонким А-cигма и С-волокнам, достигать центральной нервной системы. Рекомендуемые параметры: частота 1000-2000 Гц, длительность импульсов – 0,15-0,20 мсек, величина среднего тока – от 0,1 до 3,0 мА. Длительность процедуры электрообезболивания составляет 40-60 минут 1 раз в день в первые трое суток заболевания. Аналгетическое действие развивается не сразу, а через 10-15 минут [37]. Эффект одной процедуры сопровождается длительным аналгетическим последействием (2-24 часа).
Транскраниальная электроаналгезия позволяет получить достаточный уровень обезболивания у большинства больных ИМ (купирующий эффект 84,3%) [41]. При этом отмечается нормализация артериального давления, частоты сердечных сокращений и дыхания. Методика достаточна эффективна и безопасна, практически нe имеет противопоказаний.
Большим достижением в обезболивании некупирующегося ангинозного статуса стала эпидуральная блокада (ЭБ) [14, 28]. При ЭБ местными анестетиками (МА) развивается блокада передних и задних корешков спинного мозга. Взаимодействуя с мембраной нервной клетки, МА препятствуют возникновению нервного импульса и обратимо блокируют его проведение по нервному волокну. Но следует сказать, что применение ЭБ имеет определенные ограничения, связанные с развитием специфических осложнений и наличием технических трудностей при ее выполнении [26, 36, 40].
Симпатическая блокада сопровождается развитием дилатации артерий и артериол, снижением венозного тонуса, уменьшением венозного возврата к сердцу и снижением артериального давления [7]. При этом происходит значительное снижение общего периферического сопротивления (на 5-20%), ударного объема сердца (на 10-30%), артериального давления (на 15-33%) [47]. В связи с повышением тонуса парасимпатической системы и развитием рефлекса Бейнбриджа у больных развивается урежение частоты сердечных сокращений.
Фармакологическая денервация сердца и его десимпатизация в физиологических пределах оказывает благотворное влияние на систему кровобращения [6, 23]. Уменьшение коронарного кровотока, которое наблюдается после снижения среднего аортального давления, компенсируется снижением работы миокарда за счет уменьшения пред- и постнагрузки и уменьшения частоты сердечных сокращений. ЭБ МА на уровне Th1-6 способна в определенной степени увеличивать диаметр стенозированных коронарных артерий [55], не влияя при этом на их нестенозированные сегменты и не вызывая вазодилатации мелких коронарных сосудов [40]. Высокая ганглионарная блокада симпатических волокон стимулирует коллатеральное кровообращение миокарда, что может в определенных условиях способствовать улучшению питания в зоне ишемии и повреждения, снижает давление в правых полостях сердца и легочных сосудах [19].
ЭБ МА не оказывает прямого влияния на внутрисердечную проводимость даже у больных с исходными ее нарушениями. В ряде исследований отмечено, что под влиянием ЭБ происходит снижение потребления кислорода миокардом и улучшение функций левого желудочка, улучшение оксигенации артериальной крови в связи со снижением внутрилегочного венозного шунта, нормализация регионарной гемодинамики, благотворные изменения вязкостных параметров крови посредством регуляции транскапиллярного обмена [35, 46, 59].
Обычно в эпидуральное пространство (ЭП) на уровне Тh1-6 вводится 4 мл 2% лидокаина или 3-5 мл 2-2,5% раствора тримекаина [58]. Для пролонгирования эффекта введение повторяют каждые 2 часа (2-5 раз в сутки). Суточная доза может достигать 2 г [43]. ЭБ МА полностью купирует болевой синдром уже через 5-10 минут после введения препарата. Частота сердечных сокращений при этом уменьшается, в среднем, на 6-8 в минуту, систолическое артериальное давление – на 10-15 мм рт. ст. Более того, у ряда больных наблюдается быстрое обратное развитие признаков инфаркта миокарда. Недостатками ЭБ МА является относительно короткий период действия, риск повреждения спинного мозга и развитие тахифилаксии.
Открытие в центральной нервной системе опиатных рецепторов и их эндогенных лигандов позволили более эффективно использовать ЭБ для лечения болевого синдрома у больных ИМ. Введение в эпидуральное пространство (ЭП) минимальных доз НА вызывает длительную и избирательную блокаду болевой импульсации и практически не влияет на другие виды чувствительности [25, 28, 53].
В нашей стране для эпидурального введения из НА разрешены морфин, фентанил и промедол. Для ЭБ морфин используется в дозе 2-5 мг, фентанил – 0,05-0,1 мг, промедол – в дозе 10-20 мг [40]. Эпидуральное введение морфина в дозе 2-4 мг эффективно подавляет болевой синдром у больных в остром периоде ИМ [12, 24]. Пункция и катетеризация ЭП обычно производится на уровне Тh1-6. Полное исчезновение боли наблюдается через 10-15 минут, продолжительность действия – 18-24 часа [16]. В эксперименте выявлено, что увеличение дозы НА существенно не усиливает глубину аналгезии, но увеличивает ее длительность [57]. Первоначальная доза морфина до 2 мг не всегда и не у всех больных приводит к полному купированию болевого синдрома [38]. Увеличение дозировки морфина свыше 4-5 мг на одно введение также нецелесообразно, так как сопровождается усилением нежелательных эффектов, не приводя к существенному увеличению качества обезболивания [40].
При эпидуральном введении НА у больных ИМ происходит нормализация показателей гемодинамики и внешнего дыхания, снижение количества катехоламинов, увеличение почасового диуреза и улучшение показателей электрокардиограммы в динамике [39]. Через 1 час после введения отмечается восстановление физиологического равновесия между симпатическим и парасимпатическим отделами вегетативной нервной системы [11]. Эпидуральная аналгезия морфином в дозе 2-5 мг оказывает положительное влияние на биомеханику дыхания и газообмен [8, 10]. ЭБ НА в грудном отделе позволяет значительно улучшить качество обезболивания и увеличить его продолжительность при купировании болевого синдрома [10]. Но широкому внедрению в практику препятствует ряд факторов: 1) высокий риск повреждения спинного мозга; 2) возможность развития отсроченной депрессии дыхания; 3) необходимость привлечения высококвалифицированных анестезиологических кадров. Для снижения риска проведения аналгезии была разработана методика проведения ЭБ НА у больных ИМ в люмбальном отделе [5, 13].
Интерес к использованию "люмбальной" ЭБ НА в интенсивной терапии ИМ объясняется технической простотой и безопасностью пункции-катетеризации ЭП в поясничном отделе, где его размеры максимальны (9,8-10,2 мм) и она проводится ниже окончания спинного мозга [38]. Возможность применения эпидурального введения НА в люмбальном отделе базируется на исследованиях проницаемости твердой мозговой оболочки, в зависимости от уровня введения и распространения опиатов в ростральном направлении со спинномозговой жидкостью, проведенными И.А. Витенбеком [17, 18]. Пункция ЭП производится в поясничном отделе позвоночника (L2-3) по общепринятой методике. Для снижения риска развития отсроченной депрессии дыхания НА вводятся в 10 мл 0,9% раствора NaCl [17, 18]. Длительность нахождения катетера в ЭП зависит от наличия болевого синдрома и необходимости эпидурального введения НА (в среднем 3-7 дней). Проведение блокады в люмбальном отделе полностью исключает возможность случайной травмы спинного мозга, уменьшает вероятность перфорации твердой мозговой оболочки и интратекального введения аналгетика, облегчает процедуру пункции и катетеризации ЭП [52, 53].
При погрешностях в технике проведения ЭБ возможна перфорация твердой мозговой оболочки и случайное интратекальное введение препарата, ранение венозного сплетения или спинномозгового корешка [40]. При нарушении принципов асептики могут развиться гнойные осложнения. Помимо этого, ЭБ НА имеет специфичные побочные эффекты. Это депрессия дыхания, транзиторная задержка мочеиспускания, кожный зуд, тошнота, рвота [38].
Основной опасностью при эпидуральной блокаде является незамеченная пункция твердой мозговой оболочки с последующем введением значительного количества МА или НА в субарахноидальное пространство [37]. Истечение ликвора является очевидным признаком субарахноидальной пункции. При этом истечение идет с постоянной частотой капель, и ее температура равна температуре тела. При подозрении на перфорацию твердой мозговой оболочки следует иглу извлечь и снова ввести на сегмент выше или ниже. Для определения характера вытекающей по катетеру жидкости можно использовать пробу с 25% сульфосалициловой кислотой или с лакмусовой бумажкой [40]. При развитии тотального спинального блока основные усилия должны быть направлены на немедленное проведение искусственной вентиляции легких и быстрое достижение вазопрессорного эффекта [38]. ЭБ необходимо проводить в случаях если имеется [11]:
1. Болевой синдром, оцениваемый не менее чем в 4 балла, при том, что внутримышечные и/или внутривенные введения НА не дали полного обезболивающего эффекта (интенсивность боли оценивается по 5-балльной шкале).
2. Затяжное течение инфаркта миокарда.
3. Рецидивирующий инфаркт миокарда.
4. Наличие в М-комплексе на ЭКГ зубца S+ на фоне высокой интенсивности болевого синдрома, что специфично для угрожающего разрыва миокарда.
5. Эпистенокардитический перикардит или формирующаяся острая аневризма сердца с выраженным болевым синдромом.
Противопоказания к проведению эпидуральной анестезии делятся на абсолютные и относительные. Абсолютными противопоказаниями принято считать:
1) воспалительные изменения в области предполагаемой пункции;
2) наличие генерализованной инфекции (сепсис);
3) тяжелый шок (обосновано использование ЭБ НА на фоне параллельно проводимой интенсивной терапии);
4) повышенную чувствительность к препаратам для проведения эпидуральной блокады.
К относительным противопоказаниям относят:
1) деформации или другие изменения позвоночника, создающие препятствия для выполнения пункции-катетеризации эпидурального пространства;
2) заболевания центральной или периферической нервной системы;
3) глубокую артериальную гипотонию (тяжелая сердечно-сосудистая недостаточность);
4) гипокоагуляцию.
В связи с усовершенствованием методики проведения эпидуральной блокады и получением новых клинических данных, круг противопоказаний может сужаться. Так, долгое время антикоагуляционная терапия считалась противопоказанием к проведению эпидуральной анестезии из-за риска развития эпидуральной гематомы. Ряд исследований и наш собственный опыт проведения ЭБ на фоне антикоагулянтной терапии у больных ИМ свидетельствует о незначительном риске развития этого осложнения у исследуемой категории пациентов [13].
М.М. Ожегова, В.К. Ожегов
Новогрудское ТМО, кардиологическое отделение – ОАРИТ
В 1996 году сердечная патология была ответственна за большее число смертей, чем цереброваскулярные нарушения, рак легкого, рак молочной железы и СПИД вместе взятые [Ventura SJ, Peters KD, Martin JA, et al. Births and decaths: United States, 1996. Mon Vital Siat Rep 1997, 46 (1 Suppl 2): 1-40].
Острый коронарный синдром включает целый спектр сердечных приступов – от нестабильной стенокардии до инфаркта миокарда.
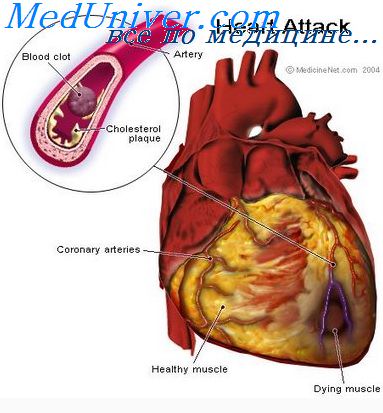
В основе лежит окклюзии просвета одной из эпикардиальных коронарных артерий тромбом. Последнее приводит к некрозу кровоснабжаемого артерией участка сердечной мышцы вследствие несоответствия притока кислорода и субстратов метаболизма к миокарду и потребностью в них [Л.И. Ольбинская, П.Ф. Литвицкий. Коронарная и миокардиальная недостаточность. М., Медицина,1986]. Объем некроза зависит в первую очередь от длительности и стойкости прекращения тока крови по сосуду (хотя значение имеют и некоторые другие факторы – наличие и выраженность коллатерального кровообращения, потребность миокарда в кислороде в момент окклюзии и т.д.).
Механизм развития боли принято объяснять следующим образом.
На ранних этапах гипоксии и ишемии миокарда значительно уменьшается содержание калия в кардиомиоцитах в связи с выходом его из клетки в межклеточное пространство. Кроме того, в миокарде начинает преобладать анаэробный гликолиз, вследствие чего накапливаются молочная кислота, водородные ионы, развивается ацидоз. Эти процессы сопровождаются накоплением в миокарде таких биологически активных веществ, как аденозин, брадикинин, гистамин, серотонин, нейропептид Р. Эти вещества вызывают раздражение рецепторов миокарда и окончаний симпатического и блуждающего нервов. Импульсы от чувствительных окончаний внутрисердечных нервов достигают сердечного сплетения и затем передаются к симпатическим ганглиям, расположенным на уровне C7-Th4. Далее импульсы передаются в гипоталамус и кору головного мозга – основные высшие центры, активация которых формирует ощущение боли. Нейропептид Р значительно облегчает передачу боли в высшие воспринимающие центры. Интенсивность боли зависит также от уровня содержания в ЦНС эндогенных опиатов – эндорфинов и энкефалинов и, как следствие, функционального состояния опиоидергической системы мозга [А.Н.Окороков. Диагностика болезней внутренних органов. т.6. М. Медицинская литература, 2002.].
Проблема обезболивания – одна из важнейших при лечении ОКС. Конечный результат интенсивной терапии во многом зависит от эффективности аналгезии [Альперт Д., Френсис Г. Лечение инфаркта миокарда (пер. с англ.). М., Практика, 1994.; Бабкин А.П., Усков В.М., Владыкина Н.Н. Новое в диагностике, лечении. / Сборник научных трудов. Воронеж. 1991. С.24-26.]. Чем выраженнее и продолжительнее болевой синдром, тем больше опасность развития тяжелых осложнений [Рябов Г.А. Синдромы критических состояний. М., Медицина, 1994.; Сумин С.А. Неотложные состояния. Москва, "Литера", 1997.]. Главной задачей обезболивания является смягчение стрессорной реакции при минимальном угнетающем действии медикаментов на системы кровообращения и дыхания. Снижение или полное купирование болевого стресса способствуют уменьшению числа осложнений и более благоприятному течению заболевания [Kaul S., Abbot R.D. Annals of Intensive Medicine. 1994. Vol. 121. P. 967-968.]. В настоящее время для купирования болевого синдрома у больных ИМ используется большое количество лекарственных средств с различными механизмами действия [Храмов В.В., Чаплинский С.В., Сушарин Л.Н., Лемехов П.Г. Тезисы докладов и сообщений 6-го Всероссийского съезда анестезиологов и реаниматологов, Москва, 1998. С.249.].
Опиоидные (наркотические) аналгетики (НА)
Термином “опиаты” обычно обозначают вещества, извлекаемые из опия: морфин, кодеин, а также полусинтетические соединения, которые получают на основе указанных алкалоидов или тебаина, также содержащегося в опии. Опиоидами называют все вещества естественного и синтетического происхождения, взаимодействующие с опиоидными рецепторами и имеющими сходство с морфином по фармакологическим свойствам [Goodman and Gilman’s the Pharmacological Basic of Therapeutics/ – 9-th Ed./ Eds-in-chief J.G. Hardman, L.E. Limbird. – 1996.].
Фармакологические эффекты опиоидных аналгетиков обусловлены их взаимодействием с опиоидными рецепторами в ЦНС и периферических тканях. Морфин, фентанил, алфентанил, суфентанил и др. составляют группу агонистов опиоидных рецепторов, проявляя наибольшее сродство к μ-рецепторам. Бупренорфин, буторфанол, налбуфин, пентазоцин относятся к группе частичных агонистов и агонистов-антагонистов опиоидных рецепторов. Различные эффекты опиоидных аналгетиков связывают с возбуждением разных подтипов опиоидных рецепторов [В.В. Чурюканов. Болеутоляющие средства: Сравнительная оценка, механизмы действия, перспективы. //Анест. и реаниматол.- 1998.-№5.-С4-11.].
Морфина гидрохлорид является основным представителем группы НА. Обладает мощной аналгетической активностью, вызывает чувство эйфории, устраняет тревогу и страх, вызывает дилатацию периферических артерий и вен (“бескровную флеботомию”), но угнетает дыхание и усиливает активность рвотного центра. Бесспорным достоинством препарата является уменьшение гемодинамической нагрузки на сердце за счёт снижения пред- и постнагрузки [В.В.Руксин. Неотложная кардиология. Санкт-Петербург. Невский диалект. 2000.]. Используется внутривенно в дозе 3-5 мг, при необходимости и отсутствии нарушений дыхания или других побочных эффектов, повторно вводят по3-5мг морфина до суммарной дозы 10 мг; внутримышечно или подкожно – 10-20 мг. Наибольший обезболивающий эффект развивается в зависимости от способа введения через 30-60 минут. Полного обезболивания обычно удается достичь в 15-30% случаев, неполного – в 40-60%.
Другим НА, часто используемым для обезболивания ИМ, является промедол. Препарат по своим свойствам близок к морфину, но меньше угнетает дыхательный центр, меньше возбуждает рвотный центр и центр блуждающего нерва. Разовая доза при внутривенном и внутримышечном введении у больных ИМ составляет 10-20 мг.
Наиболее популярным НА является фентанил [Яикин Ю.М., Плотникова Н.Д., Гольберг Г.А. Догоспитальный этап острого инфаркта миокарда. / Под ред. Р.С. Карпова. Томск, Изд. Томского университета, 1993.]. Это синтетический НА, с выраженным аналгетическим действием (в 100 раз превосходит морфин). При внутривенном введении препарата в дозе 0,05-0,1 мг (1-2 мл 0,005% раствора) эффект наступает через 1-3 минуты и продолжается в течение 15-30 минут [Сыркин А.Л. Инфаркт миокарда. М., Медицина. 1998.]. Характеризуется коротким периодом действия (около 30 минут). При внутривенном введении в дозе 0,1-0,5 мг может вызвать резкое угнетение дыхания, ригидность грудной клетки, брадикардию.
В последние годы для обезболивания ИМ используются пентазоцин, налбуфин, трамадол [Лебедева Р.Н., Никода В.В. Фармакотерапия острой боли. М., АИР-АРТ, 1998.]. Пентазоцин (фортрал) является слабым антагонистом опиатов. Способен снимать угнетающее действие на дыхание фентанила, сохраняя аналгезию. Длительность аналгезии при введении препарата в дозе 30 мг в среднем составляет 3-4 часа. Увеличение дозы более 30 мг обычно не влечёт большее угнетение дыхания, однако при этом возрастает частота возникновения дисфории и других психомиметических эффектов. В отличие от морфина пентазоцин может вызывать повышение артериального давления и тахикардию, что ограничивает применение препарата при ИМ [В.В. Чурюканов. Болеутоляющие средства: Сравнительная оценка, механизмы действия, перспективы. //Анест. и реаниматол.- 1998.-№5.-С4-11.]. Налбуфин (нубаин) является аналгетиком синтетическою ряда. По фармакодинамике схож с пентазоцином. В отличие от последнего мало влияет на сердечно-сосудистую систему, не оказывает гипердинамического действия на кровообращение [В.С. Литовченко, А.В. Блинов. Применение морадола и нубаина для купирования болевого синдрома у больных ИБС. //Анест. и реаниматол.- 1998.-№5.-С.30-31.]. Обезболивающий эффект после внутривенного введения 10-20 мг наступает через 3-5 минут, после внутримышечного – через 5-10 минут. Длительность эффекта – 4-6 часов. Препарат вводится, в среднем, 3-4 раза в сутки [Литовченко B.C. Тезисы докладов и сообщений 6-го Всероссийского съезда анестезиологов и реаниматологов. / Москва, 1998. С.156.]. Хорошие результаты обезболивания ИМ отмечаются при использовании трамадола в средней дозе 1,4 мг/кг (достигнуто достаточное обезболивание в 58,8% случаев) [Лебедева Р.Н., Никода В.В. Фармакотерапия острой боли. М., АИР-АРТ, 1998.]. Препарат более безопасен по сравнению с морфином и промедолом, мало угнетает дыхание, существенно не влияет на желудочно-кишечный тракт, обладает значительно меньшим наркогенным потенциалом, поэтому его более целесообразно использовать у больных пожилого возраста с умеренным болевым синдромом или с сердечной недостаточностью [В.В. Чурюканов. Болеутоляющие средства: Сравнительная оценка, механизмы действия, перспективы. //Анест. и реаниматол.- 1998.-№5.-С4-11.].
При купировании болевого синдрома у больных ИМ необходимо блокировать не только центральные, но и клеточные, эндокринные и вегетативные реакции организма на повреждающие воздействия [Мажерова О.П., Олесин А.И. Прогнозирование и лечение жизненно угрожающих осложнений острого инфаркта миокарда на догоспитальном этапе и в клинике. / Метод, рекомендации. Л., ЛНИИС, 1991.]. Эта задача может быть решена с помощью НЛА – сочетанного применения аналгетика и нейролептика. НЛА оказывает селективное воздействие на клетки зрительного бугра, подбугорной области, ретикулярную формацию, вызывая потерю болевой чувствительности, состояние психического и двигательного покоя без наступления сна. В качестве нейролептика обычно используется дроперидол [Сыркин А.Л. Инфаркт миокарда. М., Медицина. 1998.]. Препарат вызывает выраженное нейровегетативное торможение, оказывает противошоковый эффект, обладает противорвотным действием [Малая Л.Т. Неосложненные и осложненные формы заживления инфаркта миокарда. Киев, Здоровье, 1992.], Аналгетическим компонентом чаще всего служит фентанил, но может использоваться другой препарат (трамадол, ненаркотические аналгетики). Существует готовая смесь – таламонал, которая содержит 0,05 мг фентанила и 2,5 мг дроперидола в 1 мл. Обезболивающий эффект НЛА можно усилить предварительным введением 10-15 тыс. ЕД гепарина [Голиков А.П. Сб. статей, посвященных 75-летию со дня основания Станции скорой и неотложной медицинской помощи города Москвы. 1994. С. 19-22.].
НЛА обеспечивает хорошее обезболивание у большинства больных. У больных пожилого и старческого возраста с выраженной сопутствующей соматической патологией при использовании классической НЛА выявляются нарушения функции внешнего дыхания [Дзизинский А.А., Тумак В.Н., Бидагаев В.Б. Анестезиология и реаниматология, 1990. N5. С. 43-45.; Закин А.М. Нейролептанальгезия в остром периоде инфаркта миокарда под контролем функции дыхания. Автореф. дис. канд. мед. наук. М., 1979.]. Чтобы при проведении НЛА избежать угнетения дыхания, целесообразно усиливать ненаркотический компонент (анальгин, баралгин, трамадол и т.п.) [Яикин Ю.М., Плотникова Н.Д., Гольберг Г.А. Догоспитальный этап острого инфаркта миокарда. / Под ред. Р.С. Карпова. Томск, Изд. Томского университета, 1993.].
Атаралгезией называют метод комбинированного использования транквилизаторов и НА (например, 2 мл 0,005% раствора фентанила и 2 мл 0,5% раствора диазепама) [Сумин С.А. Неотложные состояния. Москва, "Литера", 1997.]. Клиника атаралгезии сходна с клиникой нейролептаналгезии, но характеризуется меньшими нарушениями дыхания и гемодинамики, что позволяет широко использовать данную методику у больных пожилого и старческого возраста с выраженной сопутствующей патологией [Сумароков А.В., Моисеев B.C. Клиническая кардиология. / Руководство для врачей. М., 1995. С. 38.]. Наибольшее применение для атаралгезии из транквилизаторов получил диазепам [Руксин В.В. Основы неотложной кардиологии. Л., АООТ "Эвеланш". 1994.; Провоторов В.М., Усков В.М., Барташевич Б.И. Инфаркт миокарда. Воронеж, 1999.]. Препарат не оказывает прямого влияния на миокард, но кратковременно уменьшает общее периферическое сопротивление, благодаря чему может несколько снижаться артериальное давление и сердечный выброс. Препарат параллельно с торможением поведенческих проявлений ноцицептивных реакций значительно уменьшает прессорные реакции артериального давления и тахикардию, усиливает кардиохронотропный эффект барорефлекса и модулирующую функцию "аналгетических" систем среднего мозга. В качестве аналгетика чаще всего используются фентанил, промедол, пентазоцин в обычных или несколько уменьшенных дозировках (возможно использование других препаратов) [Кузнецова О.Ю., Михайлович В.А., Руксин В.В. Болевой синдром / Под редакцией В.А. Михайловича, Ю.Д. Игнатова. Л.: Медицина, 1990. С. 189-205.].
Клонидин – водорастворимый препарат, легко проникающий через гематоэнцефалический барьер. Обладает селективными α-2-адреностимулирующими свойствами. Имеющиеся данные позволяют рекомендовать препарат для включения в комплекс аналгетических средств, используемых при болевом синдроме у больных с инфарктом миокарда [Кузнецова О.Ю., Михайлович В.А., Руксин В.В. Болевой синдром / Под редакцией В.А. Михайловича, Ю.Д. Игнатова. Л.: Медицина, 1990. С. 189-205 .]. Помимо обезболивающего эффекта клонидин способен обеспечивать уменьшение работы поврежденного миокарда путем уменьшения адренергических воздействий на сердце. Использование препарата показано у больных с артериальной гипер- и нормотензией. Его применение ограничено при наличии артериальной гипотензии. По мнению В.А. Михайловича и соавт., клонидин, обладающий одновременно аналгетическим и гемодинамическим свойствами, может занять промежуточную позицию между собственно аналгетическими препаратами и специфическими способами лечения ИМ, в основе действия которых лежит уменьшение нагрузки на миокард.
Средства для ингаляционного наркоза.
Наиболее широко для обезболивания у больных ИМ использовалась закись азота [Сыркин А.Л. Инфаркт миокарда. М., Медицина. 1998.]. Аналгезирующее действие закиси наступает при концентрации 35-45 об.%. Утрата сознания наблюдается при концентрации, равной 60-80%, но не у всех пациентов. Закись азота обладает достаточным аналгетическим эффектом при купировании болевого синдрома у большинства пациентов с ИМ. В концентрациях до 80% она практически безвредна для организма. Использование более высоких концентраций ведет к развитию гипоксии. Хотя закись азота принято считать одним из традиционных способов обезболивания при ИМ, в настоящее время имеется ряд публикаций, заставляющих более осторожно подходить к ее использованию. Выявлено, что закись азота способна вызывать сужение эпикардиальных коронарных артерий и усугублять повреждение сердечной мышцы с последующим уменьшением насосной функции сердца [Trekova N., Kojevnicova V., Flerov E. Book of abstracts, 8th European congress of anesthesiology. / Warsaw, 1990. 4/6.1 -3.].
Другие средства для ингаляционного наркоза (пентран, трилен и др.) в настоящее время используются редко для проведения обезболивания у больных ИМ или применяются по определенным показаниям (необходимость выключения сознания при кардиоверсии, выполнении болезненных манипуляций, проведении искусственной вентиляции легких и т.п.) [Провоторов В.М., Усков В.М., Барташевич Б.И. Инфаркт миокарда. Воронеж, 1999.]. Это обусловлено необходимостью использования специальной наркозной аппаратуры и специфическими особенностями препаратов (способность сенсибилизации миокарда и т.п.) [Кузнецова О.Ю., Михайлович В.А., Руксин В.В. Болевой синдром / Под редакцией В.А. Михайловича, Ю.Д. Игнатова. Л.: Медицина, 1990. С. 189-205.].
Транскраниальная электроаналгезия представляет собой воздействие электрическим током на структуры головного мозга, которое способно вызывать состояние обезболивания или снижать интенсивность болевых ощущений [Лебедев В.П. Болевой синдром. / Под редакцией Михайловича В.А., Игнатова Ю.Д. Л., Медицина. 1990. С. 162-172.]. Механизм возникновения аналгезии при электростимуляционных способах обезболивания связан с активацией эндогенных опиатных структур. Это приводит к высвобождению опиоидных пептидов, в частности, β-эндорфина, концентрация которого в плазме и спинномозговой жидкости возрастает в несколько раз. Кроме того, стимуляция толстых периферических афферентных волокон угнетает интернейроны головного мозга и не позволяет болевым импульсам, проводящимся по тонким А-cигма и С-волокнам, достигать центральной нервной системы. Рекомендуемые параметры: частота 1000-2000 Гц, длительность импульсов – 0,15-0,20 мсек, величина среднего тока – от 0,1 до 3,0 мА. Длительность процедуры электрообезболивания составляет 40-60 минут 1 раз в день в первые трое суток заболевания. Аналгетическое действие развивается не сразу, а через 10-15 минут [Провоторов В.М., Усков В.М., Барташевич Б.И. Инфаркт миокарда. Воронеж, 1999.]. Эффект одной процедуры сопровождается длительным аналгетическим последействием (2-24 часа).
Транскраниальная электроаналгезия позволяет получить достаточный уровень обезболивания у большинства больных ИМ (купирующий эффект 84,3%) [Руксин В.В. Основы неотложной кардиологии. Л., АООТ "Эвеланш". 1994.]. При этом отмечается нормализация артериального давления, частоты сердечных сокращений и дыхания. Методика достаточна эффективна и безопасна, практически нe имеет противопоказаний.
Параллельно с купированием болевого синдрома проводятся все остальные лечебно-диагностические мероприятия:
- Восстановление коронарного кровотока.
- Уменьшение работы сердца и потребности миокарда в кислороде.
- Ограничение размеров инфаркта миокарда.
- Лечение и профилактика осложнений инфаркта миокарда.
 26-07-2019
26-07-2019 0 Просмотров
0 Просмотров 0 комментариев
0 комментариев 0 Рейтинг
0 Рейтинг