
Кабардино-Балкарский государственный университет им. Х.М. Бербекова, медицинский факультет (КБГУ)
Уровень образования — Специалист
Сертификационный цикл по программе «Клиническая кардиология»
Московская медицинская академия им. И.М. Сеченова
Порок сердца – достаточно серьезная патология, при которой нарушается работа клапанного аппарата. Комплексность выраженности симптоматики включает стеноз, микропороки комбинированного и сочетательного типа, развитие сердечной недостаточности. Подобные факторы при отсутствии надлежащей терапии могут привести к тяжелой форме инвалидности или летальному исходу. Именно поэтому важно вовремя провести диагностику и приступить к лечению.
Что нужно знать о проблеме?
В случае серьезных нарушений структуры сердца функционирование жизненно важного органа дает сбои и, следовательно, начинает страдать весь организм. Порок сердца – это поражение сердечных клапанов или его структур.
Врожденный характер выявляется в ходе осмотра пациента. Такая форма является частой причиной инвалидности и летального исхода в молодом возрасте. Что провоцирует патологию? Основной причиной является ревматизм (90% случаев), атеросклероз (около 6%) и другие болезни (травмы, опухоли).
Врожденные пороки – большая и разнообразная группа заболеваний сердца и крупных сосудов. Сопровождаются изменением кровотока, перегрузкой и сердечной недостаточностью. Диагностируется у 1-2% всех новорожденных. Ряд характерных признаков позволяет диагностировать заболевание.

Выраженность клинической картины: полное описание симптоматики
Симптомы, которые говорят о том, что у человека такой вид патологии, обширны. Проявление клинической картины общее для врожденной и приобретенной формы болезни. Порок сердца отличается следующими признаками.
- Нарушение мозговой деятельности. Человеческий мозг из-за нарушения кровотока начинает обрабатывать информацию в замедленном режиме. У детей наблюдается заторможенность в развитии, а у взрослых – плохое восприятие обычных жизненных процессов. Человек плохо складывает числа, часто забывает слова и другую простую информацию.
- Синюшность кожных покровов или излишняя бледность. Синеватый оттенок проявляется в районе носа, ушей или по всему телу.
- Изменение формы пальцев на руках и выпуклость ногтя – порог сердца можно диагностировать, обратив внимание на пальцы рук. Если у человека есть проблемы с кровотоком, то их кончики сильно раздуваются, а ногти приобретают выпуклую форму (напоминают стекла часов).
- Учащенное дыхание, частое переутомление. После физических нагрузок наблюдается сильная отдышка. Слабость, которая возникает каждые 2-3 часа, также говорит о проблемах с сердцем.
- Частые обмороки. Этот признак свидетельствует о запущенной форме. При появлении частых потерь сознания без видимых на то причин (или после занятий спортом) нужно срочно обратиться за медицинской помощью.
Среди смежных симптомов – легкий кашель. Также больной может отхаркиваться кровью. В исключительных случаях у людей с таким диагнозом развивается мерцальная аритмия (нарушение сердечного ритма) и отек легких.

При пороках сердца любых типов отсутствует активность в физическом плане. При любых нагрузках заметно увеличивается сердечный ритм. Кровь начинает «бегать» по организму быстрее, снабжая питательными веществами задействованные мышечные ткани. Больное сердце при этом плохо справляется с такой задачей.
Стадии патологии и специфика выраженности симптомов
Выраженность клинической картины зависит от стадии нарушений работы сердца в организме.
- Компенсаторная. Полное отсутствие выраженности недуга. Сердце вырабатывает приспособительные механизмы и самостоятельно корректирует нарушения. Организм адаптируется к имеющимся проблемам.
- Стадия субкомпенсации. Признаки проявляются после малейших физических нагрузок (быстрая ходьба). У больного начинается одышка, учащается пульс, появляется цианоз (фиолетовый или синий оттенок кожи), отечность, предобморочное состояние.
- Затем наступает фаза декомпенсации. Компенсаторные функции сердца истощены, типичные симптомы проявляются в состоянии полного покоя. Из-за затрудненного перекачивания крови одышка сопровождает больного даже в лежачем положении. Происходят дистрофические изменения в организме.
- Последняя стадия – терминальная. Летальный исход.
Установка точного диагноза: специфика выявления недуга в детстве
Диагностика по выявлению такой сердечной патологии обычно начинается еще с профилактического обследования женщины, в утробе которой развивается ребенок. Прослушивание сокращений и работы сердца дает возможность определить порок сердца у младенца на ранней стадии развития. Как только ребенок появляется на свет, врачи проводят осмотр, прослушивают шумы сердца, наблюдают в первые дни жизни. Если появляется необходимость – новорожденного переводят в специальные центры.

Профилактическая диспансеризация дошкольников и школьников включает осмотр детским врачом-педиатром и полную проверку сердца. Если у ребенка обнаруживают неясные шумы, то его направляют на обследование к кардиологу, который проводит ряд лабораторных и инструментальных процедур.
Наиболее эффективным методом проведения диагностики шумов сердца принято считать фонокардиографию. Благодаря этому виду исследования можно сделать запись и последующую расшифровку звуков. Метод дает возможность различить органические и функциональные шумы.
Подробная характеристика методов диагностики
Если после ознакомления со списком симптомов, вы нашли совпадения с собственной ситуацией – лучше перестраховаться и обратиться в клинику, где порок сердца выявит точная диагностика.
Первоначальный диагноз можно определить с помощью пульса (измерять, находясь в состоянии покоя). Методом пальпации проводиться осмотр пациента, слушают сердцебиение для выявления шумов и изменения тона. Также проверяются легкие, определяется размер печени.
Список инструментальных способов для подтверждения диагноза включает ряд процедур.
- УЗИ – универсальный и проверенный метод. Только с его помощью можно обнаружить порок сердца у малышей еще до их рождения. Является профилактической мерой и делается несколько раз для получения или подтверждения результата. Полученная информация помогает понять работу различных отделов сердца, определить утолщенные участки мышц и выявить обратный заброс крови.
- Фотокардиография – исследования состояния сердечной мышцы, построенное на комплексном прослушивании шумов в процессе его функционирования.
- Рентген – метод, основанный на графической оценке размеров сердца и наличия лишней жидкости в плевральных полостях. Для получения информации анализируется снимок грудной клетки человека.
- Томография. При помощи специального оборудования доктор проводит исследование. Принцип действия построен на резонансе. В настоящий момент проводится за считанные минуты с помощью компьютера. Применяется для выявления редких форм врожденных пороков.

Электрокардиограмма проводится в обязательном порядке. Такая процедура представляет собой комплексный анализ миокарды (главного мышечного слоя) и нервов, которые обеспечивают правильную работу сердца.
Наиболее распространенный метод диагностики – рентген. Такое исследование дает возможность провести анализ расширения определенных частей аорты и самого сердца. В некоторых случаях в процессе проведения применяется контрастирования пищевода. Пациент глотает контрастное вещество, а врач-рентгенолог следит за его продвижением по организму. При анатомических дефектах увеличение камеры сердца может вызвать отклонение пищевода. По этому признаку и устанавливается окончательный диагноз.
Электрокардиография: все о методе
Этот метод относится к наиболее эффективным и достоверным. Электрокардиография (ЭКГ) – метод, который представляет собой графическое изображение сокращения сердечной мышцы. Для снятия ЭКГ используют пластины, которые укладывают на поверхность тела человека (ноги, запястья, грудную клетку) и подключают к прибору. Аппарат выдает график, который напечатан на листе бумаги. Он рассматривается специалистом, который делает заключение.
Применение ЭКГ при пороках сердца помогает выявить ряд показателей:
- установить точный ритм сердечной мышцы;
- определить наличие аритмии, блокад и ишемий;
- анализ толщины сердечной мышцы;
- наличие обратного запроса крови.
Такой метод при патологиях различных типов дает возможность сделать качественную оценку работы всех клапанов и отделов сердца.
Точности при постановке диагноза помогают добиться смежные методы: эхокардиография, МСКТ или МРТ сердца. В обязательном порядке нужно пройти лабораторные исследования для установки уровня сахара и холестерина. Сдаются анализы крови и мочи, исследуют биохимический состав крови.
Помните, что диагноз о пороке сердца не является смертельным. Главное вовремя его обнаружить. Ряд диагностических методов и комплексная терапия минимизирует риски опасных осложнений и вернет пациента к нормальной и полноценной жизни.
Врожденные пороки сердца (ВПС) являются одной из самых частых форм пороков развития (22% от всех врожденных пороков развития) и встречаются с частотой 8–12 на 1 тыс. живорожденных детей. За последние 10 лет отмечается неуклонный рост ВПС – этому способствуют ухудшение экологической обстановки, «старение» беременных, рост наследственной, инфекционной патологии и другие факторы. В то же время увеличивается число более сложных и тяжелых пороков сердца.
Эмбриогенез сердца происходит в период с 3 по 9-ю неделю беременности. Воздействие на женщину неблагоприятных факторов может нарушать дифференцировку сердца и приводить к формированию ВПС. Такими факторами принято считать:
1) инфекционные агенты (вирус краснухи, цитомегаловирус, вирус простого герпеса, вирус гриппа, энтеровирус, вирус Коксаки В и др.;
2) наследственные факторы (57% случаев ВПС обусловлено генетическими нарушениями, которые могут встречаться как изолированно, так и в составе множественных врожденных пороков развития;
3) соматические заболевания матери (хронические заболевания, сахарный диабет и т.д.);
4) профессиональные вредности и вредные привычки матери (хронический алкоголизм, компьютерное излучение, интоксикация ртутью, свинцом, воздействие ионизирующей радиации и т.д.).
Летальность при ВПС чрезвычайно высока: в 1-ю неделю жизни умирают 29% новорожденных, за 1-й месяц – 42%, к 1-му году – 87% детей при естественном течении порока. Средняя продолжительность жизни – 2 мес.
К наиболее часто встречающимся ВПС относят пороки «большой пятерки»:
• дефект межжелудочковой перегородки (ДМЖП);
• коарктацию аорты (КА);
• транспозицию магистральных артерий (ТМА);
• открытый артериальный проток (ОАП);
• тетраду Фалло (ТФ).
Классификация ВПС представлена в таблице.
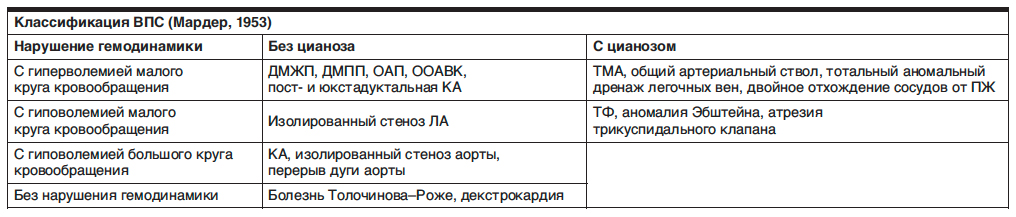
Учитывая современный уровень развития кардиохирургии, оперативная коррекция большинства ВПС выполняется, как правило, на раннем этапе, до развития выраженных нарушений гемодинамики и увеличения полостей сердца. Далее приведены некоторые особенности ЭКГ-картины, могущие наблюдаться у подобных больных.
Коарктация аорты
КА – это врожденное сегментарное сужение аорты в области дуги, перешейка, нижнего грудного или брюшного отделов. Название порока происходит от латинского coarctatus – суженный, сжатый, стиснутый. Порок относится к частым сердечным аномалиям и встречается в 6,3–7,2% случаев.
По отношению к ОАП КА подразделяется следующим образом:
1) предуктальная КА (сужение проксимальнее места отхождения ОАП);
2) юкстадуктальная КА (сужение на уровне отхождения ОАП);
3) постдуктальная КА (сужение дистальнее отхождения ОАП).
Иногда коарктация располагается в атипичном месте – на уровне нижнего грудного отдела, диафрагмы или брюшной части. Кроме истинной КА, возможны деформации аорты за счет удлинения и извилистости, однако просвет ее при этом не меняется и препятствия кровотоку нет. Такие отклонения в строении аорты называют «кинкингом».
Гемодинамика существенно зависит от типа и локализации коарктации, степени сужения, а также от наличия сопутствующих ВПС. В результате препятствия кровотоку левый желудочек (ЛЖ) гипертрофируется, причем гипертрофия развивается уже внутриутробно. Имеет место относительная коронарная недостаточность. При изолированной КА в большом круге кровообращения устанавливаются два режима кровообращения: проксимальнее (артериальная гипертензия) и дистальнее (артериальная гипотензия и дефицит кровотока) места сужения.
При постдуктальной коарктации в случае внутриутробного формирования коллатерального кровообращения течение порока бывает менее тяжелым. Коллатеральный кровоток происходит через подключичные, межреберные, внутренние грудные, лопаточные, эпигастральные и позвоночные артерии, которые со временем расширяются из-за повышенного давления в них. При неадекватном развитии коллатералей существенно повышается артериальное давление до места сужения, и кровь под давлением сбрасывается из аорты через ОАП в легочную артерию (ЛА). Величина сброса зависит от градиента между аортой и ЛА и, как правило, бывает значительной. В ответ на поступление большого дополнительного объема крови в сосуды малого круга кровообращения развиваются легочная гиперволемия и гипертензия. Аналогичная гемодинамическая ситуация отмечается и при юкстадуктальной КА.
При предуктальной КА направление шунтирования крови будет зависеть от соотношения давления в нисходящей аорте и ЛА. При выраженной степени сужения отмечается венозно-артериальный шунт крови, что приводит к появлению дифференцированного цианоза (есть на ногах, но нет на руках).
При данном пороке имеет место стеноз аорты в каком-либо ее отделе, чаще в области перешейка. Характерным гемодинамическим изменением является гипертрофия ЛЖ (ГЛЖ).
ЭКГ-признаки:
1) признаки ГЛЖ;
2) возможна блокада левой, реже – правой ножки предсердно-желудочкового пучка;
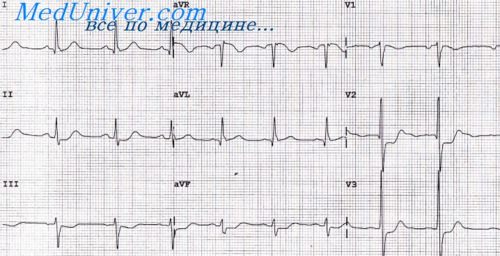
3) возможны нарушения атриовентрикулярной (АВ) проводимости (рис. 1). 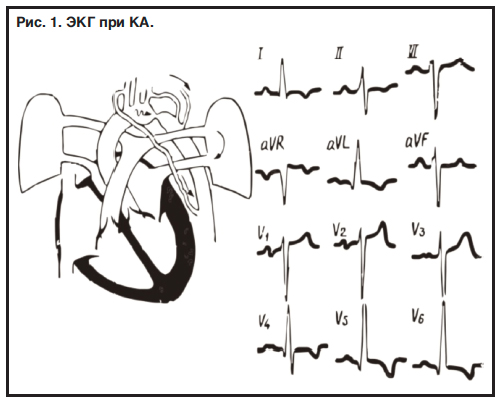
ОАП, незаращение Боталлова протока
ОАП – наличие сообщения между аортой и ЛА, считающегося аномалией в постнатальном периоде. Частота данного порока колеблется в пределах от 5 до 34%, чаще у лиц женского пола (2–4:1).
В пренатальном периоде ОАП и открытое овальное окно являются физиологическими плодовыми коммуникациями. В силу того, что малый круг кровообращения не функционирует, около 2/3 объема оксигенированной крови через ОАП поступает в нисходящую аорту. В норме вскоре после рождения в ОАП происходит спазм гладкомышечных волокон, что приводит к функциональному закрытию протока. Анатомическое закрытие, или облитерация, происходит в течение первых 2 нед постнатальной жизни. Такие патологические состояния периода новорожденности, как синдром дыхательных расстройств, врожденная пневмония, асфиксия в родах, препятствуют закрытию ОАП. Физиологическое закрытие протока задерживается у недоношенных детей, причем чем меньше гестационный возраст ребенка, тем более продолжительное время требуется для закрытия ОАП. Так, при массе тела менее 1000 г у 80% детей артериальный проток функционирует в течение нескольких месяцев.
При наличии открытого Боталлова протока сохраняется соединение между дугой аорты и стволом ЛА, при этом часть крови, проходящей из ЛЖ в аорту, поступает в легочную ЛА, затем вновь возвращаясь в ЛЖ. Патогномоничными являются диастолическая перегрузка ЛЖ вследствие прохождения через него повышенного объема крови и медленное нарастание легочной гипертензии с формированием систолической перегрузки правого желудочка (ПЖ).
ЭКГ-признаки:
1) умеренная ГЛЖ;
2) признаки перегрузки левого предсердия;
3) при присоединении увеличения ПЖ: признаки гипертрофии двух желудочков, часто в сочетании с признаками увеличения двух предсердий;
4) нарушения проводимости (АВ-блокада, блокада левой ножки предсердно-желудочкового пучка, синдром Вольфа–Паркинсона–Уайта) и ритма (политопная экстрасистолия, мерцательная аритмия);
5) в редких случаях – отсутствие ЭКГ-изменений (рис. 2). 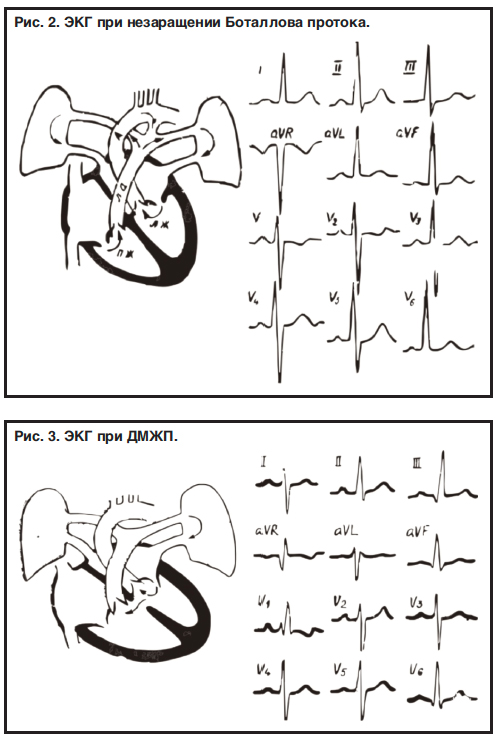
Дефект межжелудочковой перегородки
ДМЖП встречается наиболее часто, причем как в изолированном виде, так и в составе многих других пороков сердца. Среди ВПС частота данного порока варьирует от 27,7 до 42%. Одинаково часто встречается как у мальчиков, так и у девочек.
В МЖП выделяют 3 отдела: верхняя часть – мембранозная, прилегает к центральному фиброзному телу, средняя часть – мышечная и нижняя – трабекулярная. Соответственно этим отделам называют и ДМЖП, однако большинство из них (до 80%) имеют перимембранозную локализацию. На долю мышечных ДМЖП приходится 20%. По размерам дефекты подразделяют на большие, средние и малые. Для правильной оценки величины дефекта его размер надо сравнивать с диаметром аорты. Мелкие дефекты размером 1–2 мм, расположенные в мышечной части МЖП, называются «болезнью Толочинова–Роже».
В случае наличия значительного дефекта происходит шунт крови слева направо, так как давление в ЛЖ изначально больше, чем в ПЖ. Возникает легочная гипертензия, повышается нагрузка как на ПЖ, так и на ЛЖ. При очень больших размерах дефекта может произойти выравнивание давления в ПЖ и ЛЖ, в дальнейшем может поменяться направление сброса крови. При незначительных ДМЖП ЭКГ-изменения могут отсутствовать, при большом объеме шунта наблюдаются:
1) при отсутствии легочной гипертензии – ЭКГ-признаки ГЛЖ, зачастую с изменением конечной части желудочкового комплекса;
2) при нарастании легочной гипертензии – признаки гипертрофии двух желудочков;
3) ЭКГ-признаки увеличения двух предсердий;
4) возможно развитие блокады правой ножки предсердно-желудочкового пучка (рис. 3).
Дефект межпредсердной перегородки
ДМПП – это группа пороков сердца, для которых характерно аномальное сообщение между предсердиями. Данные о распространенности этого ВПС характеризуются широким диапазоном 5–37%, что связано с низкой выявляемостью ДМПП в детском возрасте (у детей до 3 лет – в 2,5% случаев, после 3 лет – 11%). У плода наличие межпредсердного сообщения не является патологической находкой и не влияет на его развитие. В подавляющем большинстве случаев ДМПП представлены вторичными дефектами (66–98%).
В МПП выделяют 2 отдела: первичную, составляющую нижнюю треть МПП, прилегающую к фиброзному телу, и вторичную – в области расположения овального окна. Соответственно отделам выделяют первичные и вторичные ДМПП. Отдельно рассматривают отсутствие МПП. Если вторичные ДМПП встречаются в изолированном виде, то первичные, как правило, входят в состав более сложных комбинированных ВПС (открытого окна АВ-канала, тотального аномального дренажа легочных вен, ТМА и т.д.).
Различают собственно ДМПП и незаращение овального окна. Небольшие дефекты могут быть гемодинамически незначимы, при значительных дефектах возникает сброс крови, как правило, из левого предсердия в правое. Таким образом, увеличивается объем крови, поступающей в ПЖ и малый круг кровообращения, вследствие чего происходит увеличение размеров правого предсердия и ПЖ. Шунт увеличивается при наличии препятствия к оттоку крови из левого предсердия (так называемый синдром Лютембаше – сочетание ДМПП с митральным стенозом), что делает гемодинамические нарушения более выраженными. 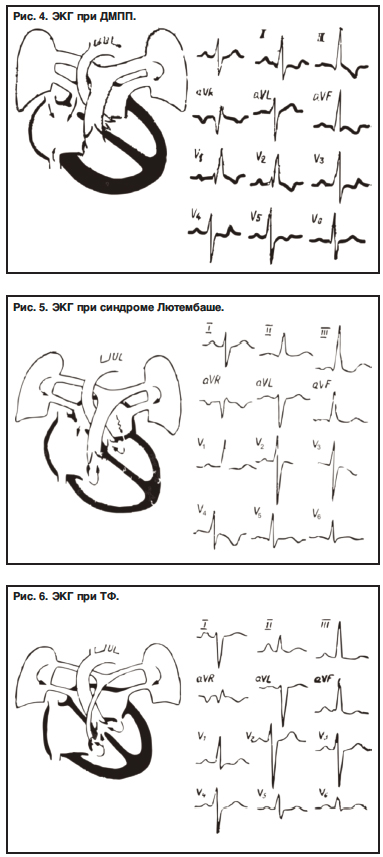
Для ЭКГ-картины при данном пороке характерно следующее (рис. 4, 5):
1) формирование высокого остроконечного зубца Р в отведениях II, III, aVF, V1, V2 (в последних двух отведениях он может быть двухфазным с преобладанием положительной фазы);
2) ЭКГ-признаки гипертрофии ПЖ (ГПЖ), блокада правой ножки предсердно-желудочкового пучка, отклонение электрической оси сердца (ЭОС) вправо;
3) замедление АВ-проводимости;
4) мерцание или трепетание предсердий, наджелудочковая тахикардия;
5) при синдроме Лютембаше – признаки увеличения двух предсердий (рис. 5).
Тетрада Фалло
ТФ относится к наиболее распространенным порокам сердца «синего» типа, составляет 12–14% всех ВПС и 50–75% «синих» пороков. Одинаково часто встречается у мальчиков и у девочек. Для данного порока сердца характерны следующие признаки:
1) сужение или атрезия ЛА;
2) высокий ДМЖП;
3) декстропозиция аорты (аорта отходит от двух желудочков);
4) ГПЖ (рис. 6).
Выделяют 3 клинико-анатомических варианта порока:
1) цианотическая форма, или «крайняя» – ТФ с атрезией устья ЛА;
2) классическая форма;
3) ацианотическая форма, или «бледная» – ТФ с минимальным стенозом ЛА.
Степень нарушения гемодинамики определяется выраженностью стеноза ЛА. Обструкция может находиться на уровне выходного отдела ПЖ, на уровне клапана ЛА, по ходу ствола и ветвей ЛА и на нескольких уровнях одновременно. Во время систолы кровь поступает из двух желудочков в аорту и в меньшем количестве – в ЛА. Вследствие того, что аорта широкая и смещена вправо, кровь по ней проходит беспрепятственно, поэтому при классической форме ТФ никогда не бывает недостаточности кровообращения. Из-за большого ДМЖП давление в желудочках одинаковое. Степень гипоксии и тяжесть состояния больных коррелируют со степенью стеноза ЛА. У пациентов с крайней формой ТФ кровь в легкие поступает через ОАП либо через коллатерали (артериовенозные анастомозы и бронхиальные артерии), которые могут развиваться внутриутробно, но чаще – постнатально. Компенсация кровообращения происходит за счет:
1) ГПЖ;
2) функционирования ОАП и/или коллатералей;
3) развития полиглобулии и полицитемии в результате длительной гипоксии.
ЭКГ-признаки:
1) отклонение ЭОС вправо (120–180°);
2) признаки ГПЖ;
3) правого предсердия;
4) нарушение проводимости по типу неполной блокады правой ножки предсердно-желудочкового пучка.
Транспозиция магистральных артерий
ТМА – ВПС «синего» типа, при котором два основных магистральных ствола расположены аномально. При этом аорта отходит от ПЖ, несущего венозную кровь, а ЛА – от ЛЖ, перекачивающего артериальную кровь. Круги кровообращения при ТМА полностью разобщены, артериальная и венозная кровь не смешиваются. Полная форма ТМА несовместима с жизнью. При наличии сообщений на разных уровнях (ОАП, ДМПП, ДМЖП) происходит частичное смешение артериальной и венозной крови, что позволяет отнести ТМА к дуктусзависимым порокам и делает ребенка жизнеспособным. ТМА входит в число распространенных ВПС «синего» типа, частота его встречаемости составляет от 4,2 до 9,9%, достоверно чаще наблюдается у мальчиков (57–88% всех случаев ТМА).
Изменения на ЭКГ зависят от размеров коммуникаций и величины легочного кровотока. Как правило, ЭОС отклонена вправо, к 3–4-й неделе жизни развиваются признаки гипертрофии правых отделов сердца либо сочетанная гипертрофия двух желудочков.
Заключение
Многообразие ВПС значительно затрудняет их диагностику. Тем не менее актуальность ранней диагностики ВПС не вызывает сомнений.
Данная публикация предназначена в помощь врачу-педиатру, кардиологу, а также врачам других специальностей.
Не следует забывать, что основную информацию о ВПС, помимо клинической картины и ЭКГ, дает эхокардиография.
Признаки гипертрофии правого желудочка следующие: изменения появляются в правых грудных отделах, что связано с увеличением размеров правого желудочка при артериальной гипертензии, что проявляется смещением вниз сегмента S—Т и появлением негативного зубца Т. Изменения на ЭКГ, в частности, в правых грудных отведениях, коррелируют с выраженной легочной гипертензией. Так, при RS-типе в отведении V1 давление в легочной артерии повышено умеренно; при RSR’-типе в отведении V1 давление не более 60—70 мм рт. ст. R-тип (qRv1 —Rv1 —Rs Vl) наблюдается при значительной легочной гипертензии.
Иногда на ЭКГ выявляется полная блокада правой ветви предсердно-желудочкового пучка.
Недостаточность левого предсердно-желудочкового клапана. В более тяжелых случаях отмечаются признаки гипертрофии левого предсердия, аналогичные изменениям при митральном стенозе.
Электрокардиограмма при стенозе устья аорты имеет большое значение для оценки тяжести порока и выраженности изменений миокарда. Электрическая ось часто располагается в нормальных пределах и лишь при значительной дилатации левого желудочка, а также v больных пожилого возраста может быть расположена горизонтально или отклониться влево.
Электрокардиограмма при недостаточности клапана аорты имеет большое значение как для оценки его тяжести, так и для определения выраженности изменений миокарда. В случае выраженного порока появляются следующие признаки изменений левого желудочка, отличающиеся от таковых при аортальном стенозе: увеличение амплитуды зубца RV1,2 и зубца Sv1,2 при этом Sv1+Rv6 или Rv6 > 35 мм; появление высоких, заостренных зубцов Т в отведениях V4, V5 и V6 и увеличенного зубца Q в отведениях V5 и V6.
Электрическая ось сердца может располагаться по-разному, у лиц молодого возраста и при нерезко выраженном дефекте — в пределах нормы; при резко выраженном пороке, а также у лиц пожилого возраста более характерно отклонение ее влево. Таким образом, главное отличие ЭКГ при недостаточности клапана аорты от таковой при аортальном стенозе — состояние конечной части желудочкового комплекса; в первом случае негативный зубец Т в сочетании с депрессией сегмента S—Т в отведениях V5, V6, I, aVL наблюдается лишь при развитии сердечной недостаточности со значительными изменениями миокарда, тогда как во втором случае эти изменения сегмента S—Т и зубца Т возможны у больных с компенсированным пороком.
Изменения комплекса QRS в ряде случаев формирует так называемый «синдром правожелудочковой дилатации». В отведении V1 и V2 комплекс QRS расщеплен, часто типа rSr’, rsP, в отведениях V4—V6 появляется значительно увеличенный зубец S; сегмент S—Tv1,2 снижен, зубец ТV1,2 двухфазный или отрицательный.
Электрокардиограмма при стенозе правого предсердно-желудочкового отверстия обнаруживает резко выраженные признаки гипертрофии правого предсердия на фоне изменений, вызванных одновременно существующими митральным и нередко аортально-мнтральным пороками.
Гипертрофия правого предсердия выражается в увеличении амплитуды заостренных зубцов Р в отведениях II, III, aVF. В отведениях V1 и V2 обычно наблюдается двухфазный зубец Р с резким преобладанием первой положительной фазы.
 26-07-2019
26-07-2019 0 Просмотров
0 Просмотров 0 комментариев
0 комментариев 0 Рейтинг
0 Рейтинг