Под определение гамма-глобулин попадают специальные сыворотки, которые вводится пациенту с целью лечения или профилактики каких-либо заболеваний инфекционного характера. Нельзя обобщать препараты этого типа. Различают такие виды: антистафилококковый гамма-глобулин, антирабический (против бешенства), антирезусный (используют в случае резус-конфликта матери и плода), противокоревый, противококлюшевый.
Когда его используют?
Известно, что в нашей стране соответствующие гамма-глобулины применяют для профилактики таких заболеваний, как корь и краснуха, гепатит А, коклюш, полиомиелит. Для этого препарат вводится внутримышечно, в последнем случае обычно перрорально Перечень заболеваний, при которых эффективным является внутривенное введение, заметно шире, среди них дерматомиозит, хронический лимфолейкоз, ВИЧ, болезнь Кавасаки, идиопатическая тромбоцитопеническая пурпура, послеоперационные осложнения (вплоть до сепсиса). В отдельных случаях препараты вводятся в спинномозговой канал.
Что собой представляет гамма-глобулин?
По сути, данные препараты являются иммуноглобулинами. Они созданы на основе белка, человеческого или животного. Могут считаться гликопротеинами. Основная функция иммуноглобулинов – защита организма от разнообразных вирусов и инфекций. На сегодняшний день в медицине используются очищенные и концентрированные препараты сывороточных белков (гамма-глобулиновая фракция). Их особенность – высокое содержание титров антител. Основная задача – создать пассивный иммунитет, который возникает в течение всего лишь нескольких часов после укола. Отметим, что этот вид иммунитета, как правило, работает не более 14 дней, в отличие от активного.
Когда вводить гамма-глобулин нельзя?
Как и у любого другого лекарственного средства, у данного препарата есть противопоказания. Их не так много, но они достаточно серьезны:
- известная повышенная чувствительность к лекарству;
- дефицит у больного IgA;
- сахарный диабет;
- нарушения в работе почек;
- беременность и период кормления грудью;
- хроническая сердечная недостаточность.
В каждом конкретном случае решение о том, является ли противопоказание абсолютным или относительным решение должен принимать врач.

Каковы побочные эффекты?
После того, как гамма-глобулин введен в организм, могут наблюдаться разного рода неприятные явления. Тошнота, рвота, головокружение, скачки артериального давления, диарея, нарушения сердечного ритма – довольно распространенные реакции. Заметно реже встречаются потеря сознания, необоснованное чувство жара или холода, гиперемия в месте укола, коллапс, анафилактический шок.
Можно ли избежать осложнений при введении?
Да, в некоторой степени. Один из постулатов – относительно медленное введение препарата. Эта тактика позволяет наблюдать состояние пациента, и вовремя среагировать, если будет выявлена непереносимость средства. Кроме того, крайне желательно, чтобы пациент не менее 1 часа после укола находился под наблюдением медиков. Во избежание порчи препарата его необходимо хранить только так, как указано производителем. В ином случае лекарство применять нельзя!
Что делать, если гамма-глобулин повышен?
Для начала следует усвоить, что нормальный показатель – от 12 до 22%. Все, что выше этой границы, считается повышением. Причиной таких показателей могут стать воспалительные процессы, хронические (в том числе, аутоимунные) заболевания.
Иммуноглобулины представляют собой белки человека (животных), которые обычно обладают свойствами антител, т.е. специфической способностью соединяться с антигеном, который стимулирует их образование. Иммуноглобулины присутствуют в крови, цереброспинальной жидкости, лимфоузлах, селезенке, слюне и других тканях, а так же в виде рецепторов на поверхностных мембранах клеток. Синтезируются они в В-лимфоцитах, содержат углеводные группировки и могут рассматриваться как гликопротеины. По электрофоретической подвижности иммуноглобулины относятся в основном к гамма-глобулинам и бета2-глобулинам. Биологическая роль иммуноглобулинов в организме связана с участием в процессах иммунитета. Их защитная функция обусловлена способностью специфически взаимодействовать с антигенами. До середины 50-х годов прошлого столетия о структурной организации иммуноглобулинов ничего не знали. Первый шаг в этом направлении сделал английский иммунохимик Р.Портер в 1959 г. Он показал, что при обработке очищенных иммуноглобулинов протеолитическими ферментами образуются три фрагмента, два из которых взаимодействуют с антигеном (патогеном) и потому названы антигенсвязывающими (Fab), и один, неспособный к такому взаимодействию (Fc).
Но это ничего не говорило о причинах их специфичности по отношению к разным антигенам. Для получения информации о молекулярных основах вариабельности нужно было значительное количество полностью идентичных белков. Сывороточные иммуноглобулины, в массе образующиеся после иммунизации, не давали такой возможности, поскольку они – производные нескольких клеточных клонов, каждый из которых продуцирует белки только одного класса и только одной, свойственной ему, специфичности. Иначе говоря, иммуноглобулины, выделяемые от иммунизированных животных, есть смесь молекул с разной специфичностью и разной принадлежностью к тому или иному классу.
Необходима была экспериментальная модель, позволяющая работать с одним клоном, образующим иммуноглобулины только одной специфичности и только одного класса. Природа предоставила такую возможность – злокачественно трансформированные плазматические клетки больных миеломой. В настоящее время существует большой набор клонированных плазмоцитов человека и животных, продуцирующих соответствующие миеломные белки.
Строение.(см. пример: строение IgG)
Изучение аминокислотной последовательности иммуноглобулинов выявило принципиальные особенности в их строении.
Молекулы иммуноглобулинов симметричны. Они построены из "легких" (около 220 аминокислотных остатков, молекулярная масса 25000 для IgG) и "тяжелых" (450-600 аминокислотных остатков, молекулярная масса для IgG– 50000) полипептидных цепей (соотв. L- (light) и Н-цепи (heavy)), скрепленных дисульфидными связями и нековалентными взаимодействиями. В антителах человека обнаружено два вида легких цепей ( и ) и пять видов тяжелых цепей ( и ), отличающихся аминокислотной последовательностью. Тяжелые цепи, характерные для каждого из классов и подклассов иммуноглобулинов, содержат по одному или более олигосахаридному фрагменту (степень гликозилированности отражается на биологических свойствах иммуноглобулинов).
Р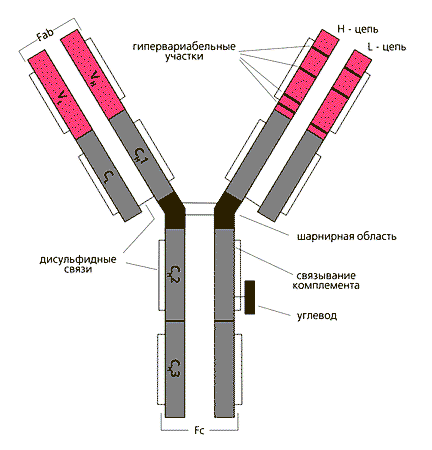 ис.1. Строение иммуноглобулина G.
ис.1. Строение иммуноглобулина G.
Две тяжелые (Н) цепи с мол. весом 50 кД и две легкие (L) с мол. весом 25 кД объединены в единую молекулу с помощью ковалентных дисульфидных связей. Каждая цепь содержит вариабельную область (VL и VH для L- и H-цепей соответственно) и константную (С), подразделяющуюся у Н-цепей на гомологичные участки (домены): CH1, CH2, CН3. L-цепь имеет один константный участок – CL. От взаимодействия VH- и VL-областей зависит специфичность иммуноглобулинов как антител. В аминокислотной последовательности V-доменов имеются гипервариабельные участки, характеризующиеся частой заменой аминокислот от белка к белку, и более консервативные. Между СН1 и СН2 доменами Н-цепи находится шарнирная область, обеспечивающая подвижность антигенсвязывающего Fab-фрагмента. СН2-домен служит местом присоединения углеводов и связывания комплемента. СН3-домен взаимодействует с Fc-рецептором (не способным связывать антиген) на поверхности клеток, принимающих участие в иммунологических реакциях.
Лёгкие цепи различных видов отличаются друг от друга С – концевой последовательностью аминокислот. С – концевая половина полипептидной цепи имеет постоянную аминокислотную последовательность, а ее N – концевая часть – вариабельную. Каждый постоянный (Сl) и вариабельный (Vl) участок легкой цепи включает 107-110 аминокислотных остатков. Тяжелые цепи построены их четырех участков – VH, C1H, C2H, C3H. Вариабельные участки их состоят приблизительно из 110-114 аминокислотных остатков, постоянные – 330.
В вариабельной части полипептидных цепей находятся определенные, так называемые "гипервариабельные участки", с наибольшим числом аминокислотных замен. В легких цепях они расположены между 24-34; 52-55; 89-97 аминокислотными остатками. Гипервариабельные участки тяжелых цепей занимают аналогичные положения, но точная локализация их пока не установлена.
Строение постоянных областей тяжелых цепей определяет эффекторные функции молекул к поверхностям макрофагов, В-лимфоцитов, тучных клеток, а также проникновение через плацентарную мембрану.
Гибкость молекул иммуноглобулинов, обеспечивающая приспособляемость к различным конфигурациям молекул антигена, обусловливается также наличием особого "шарнирного участка" в середине тяжелых цепей, содержащего много остатков аминокислоты пролина и препятствующего образованию вторичной структуры. Шарнирная область чувствительна к протеолитическим ферментам. При расщеплении ими (например, папаином) иммуноглобулин распадается на два идентичных Fab-фрагмента и один Fc-фрагмент.
В настоящее время на основании изучения первичной структуры полипептидных цепей выдвинута так называемая "доменная" гипотеза строения иммуноглобулинов, согласно которой молекулу иммуноглобулинов можно разбить на участки с относительно независимыми конфигурациями в виде глобул. Каждый домен состоит приблизительно из 100-110 аминокислотных остатков и имеет одну дисудьфидную связь, которая связывает участки цепей, образуя петлю из 60 аминокислотных остатков.
Молекулы иммуноглобулинов связанные с поверхностью лимфоцитов, имеют дополнительные гидрофобные "хвосты" на С-концах тяжелых цепей, которые встроены в мембраны клеток. Пептидные цепи иммуноглобулинов и ряда белков клеточных мембран (антигены гистосовместимости, рецепторы для антигенов Т-лимфоцитов) по своей первичной структуре сходны между собой, что указывает на общее эволюционное происхождение всех этих белков.
Связывание с антигенами.
На N-концах тяжелых и легких цепей расположены те самые вариабильные области, которые в сочетании и образуют антигенсвязывающую структуру – паратоп в составе Fab-фрагмента. Три или четыре домена со стороны С-концов тяжелых цепей составляют константную часть молекулы – Fc-фрагмент (не связывают антиген). Fc-Фрагмент состоит из четырех или шести доменов двух тяжелых цепей и определяет такие свойства иммуноглобулинов, как связывание ими комплемента, возможность проникать через плаценту, присоединяться к клеткам и фиксироваться в коже. Поскольку в состав молекулы иммуноглобулина входят две легкие и две тяжелые цепи, они формируют два паратопа (области, контактирующие с антигеном) в составе двух Fab-фрагментов, т.е. антитело бивалентно: может соединиться с двумя идентичными антигенными эпитопами. Этому способствует наличие шарнирной области между первым и вторым доменами константного фрагмента тяжелых цепей, благодаря которой обеспечивается возможность пространственной ориентации Fab-фрагментов для связывания с антигенными эпитопами. Комплекс с антигеном образуется в результате нековалентных взаимодействий, характер которых может варьировать в зависимости от специфичности антитела- связи могут быть ионными, вандерваальсовыми, водородными, при помощи солевых мостиков и гидрофобных взаимодействий.. Сила связывания с антигеном увеличивается на несколько порядков, если молекула антитела реагирует сразу двумя (или более) областями связывания с несколькими детерминантами одной молекулы антигена.
Каждая индивидуальная клетка вырабатывает антитела только одной
специфичности по правилу "одна клетка " одно антитело" (Петров , 1987). Это
означает, что в клетке активно функционируют только один вариант гена VH,
один – гена СH и по одному соответствующему гену одной из легких цепей. Все
остальные структурные гены выключены. В каждой отдельно взятой антитело-
образующей клетке из всего множества структурных генов иммуноглобулинов
функционирует их минимальное количество, необходимое для синтеза антител
одной специфичности и одного типа. Таким образом, в основе многообразия
специфичности антител лежит функционирование в лимфоидной системе большого
количества клеток и их потомков – клонов клеток – продуцентов одного вида
антител. Следовательно, количество специфичностей антител соответствует
количеству клонов клеток-антителопродуцентов, различающихся генами,
функционирующими в них.
Особенностью этих полипептидных цепей является отсутствие единого гена, кодирующего структуру всей полипептидной цепи. Всякий раз сборка такого гена происходит из отдельных сегментов. Этим обеспечивается бесконечное разнообразие структур молекул антител, способных распознать любую существующую в природе структуру антигена. Иными словами, набор (репертуар) специфических участков связывания в популяции иммуноглобулинов организма столь широк, что на любой попадающий в организм антигенный эпитоп (участок связывания) обязательно найдется строго комплементарный паратоп в составе антиген-связывающего фрагмента (Fab – фрагмента) какого-то иммуноглобулина. Поэтому говорят, что легкие и тяжелые пептидные цепи каждого класса иммуноглобулинов построены из двух основных областей – вариабельной и постоянной.
Все их антигенные детерминанты кодируются тремя несцепленными группами аутосомных генов. Одна группа кодирует тяжелую цепь
того или иного класса, другая – легкую k- типа, третья – легкую -типа. Так как полипептидные цепи состоят из двух различных участков – вариабельного (V) и постоянного (С), каждая из трех групп генов включает набор генов вариабельной – V и постоянной областей -С-гены. Таким образом, синтез каждой полипептидной цепи молекулы иммуноглобулина контролируется двумя структурными генами, а не одним, как при синтезе других белков. Один ген кодирует вариабельную область цепи, другой- постоянную. Причем существуют многие гены для вариабельных
областей полипептидной цепи, что связано с многообразием специфических

Современная медицина строится на внедрении новых форм лечения и профилактики заболеваний и на усовершенствовании старых. Что такое человеческий гамма-глобулин, инструкцию к применению, показания и противопоказания, функции и отзывы знает врач, который назначает этот препарат. Это важнейший пункт в профилактике многих заболеваний, проверенный и эффективный метод борьбы с различными патологиями их последствиями.
Что такое гамма-глобулин

Гамма-глобулин – это класс белков плазмы крови, который имеет высокую подвижность при разделении методом электрофореза. Его производят способом полной очистки плазмы, оставляя только необходимые элементы, которые будут входить в средство. Также это название лекарственного препарата, содержащего противовирусные антитела, что применяются с лечебной и профилактической целью при ряде заболеваний. Чаще всего профилактика представлена иммунизацией антителами особой фракции белка, которая имеет три основных типа гамма-глобулинов, структура которых может меняться в зависимости от конкретного заболевания.
Всего различают четыре вида человеческого иммуноглобулина:
- А класс — содержатся в крови и в секретах, принимают участие в иммунитете, создавая барьер для проникновения инфекций и токсинов;
- Е класс – принимают участие в нейтрализации токсинов, бактериолизисе и других процессах, при инфекционных заболеваниях резко повышается их содержание в крови;
- D класс – локализуются в мембране плазматических клеток, предположительно, участвуют в аутоиммунных процессах;
- G класс – наиболее важные иммуноглобулины, обеспечивают защиту организма от большинства инфекций, связывают токсины, борются с вирусами и бактериями и через плаценту передают новорожденному пассивный иммунитет, когда он отделяется от пуповины и начинает жить отдельно.
Гамма-глобулин используется как средство для иммунопрофилактики, он создает пассивный иммунитет на определенный срок, когда скорость наступления вирусов и бактерий максимальна.
Форма выпуска, состав и показания

Лекарство гамма-глобулин человека выпускается в виде раствора для внутримышечного введения в ампулах по 1,5 мл. В картонных или пластиковых упаковках содержится по 5 или 10 ампул препарата. В зависимости от дозировки действующего вещества, врач назначает разное количество капсул для курса, также значение имеет возраст пациента. Регистрационный № Р N001544/01 от 08.07.08 бессрочно.
Препарат иммуноглобулина — это концентрированный раствор иммунологически активной белковой фракции, которая выделяется при температуре ниже 0°С из плазмы крови доноров методом фракционирования этиловым спиртом. Для сдачи материал проверяется на отсутствие ВИЧ, гепатита В, антител к вирусу гепатита С и других заболеваний, которые переносятся в плазме крови.
Концентрация белка в иммуноглобулине составляет от 9,5 до 10,5%. Препарат не содержит консервантов и антибиотиков, его основная функция – повышение резистентности организма за счет активности антител.
Гамма-глобулин человека рекомендован при таких показаниях:
- профилактика гепатита А, коклюша, кори, менингококковой инфекции, гриппа и полиомиелита;
- повышение резистентности организма в период инфекционных заболеваний;
- лечение гипобулинемии.
Фармакокинетика антител достигается через 1-2 суток после введения, выведение длится 3-4 недели. Фармакодинамика — выводится через почки, после повышения уровня антител.
Читайте также 
Дозировка и инструкция по применению

Препарат вводят внутримышечно в верхний наружный квадрант ягодичной мышцы или в бедро, наружную поверхность. При введении всегда соблюдаются правила эксплуатации: если ампула хранилась в холодильнике, ее нужно выдержать при комнатной температуре в течение 2 часов. При открытии необходимо строго соблюдать все правила антисептики, а во избежание образования пены его надо набирать иглой с широким просветом.
Ранее открытую и не использованную ампулу необходимо утилизировать, также подлежит утилизации препарат с измененным цветом, осадком и истекшим сроком годности. Дозировка гамма-глобулина зависит от назначения врача.
Профилактика гепатита А:
- детям 1-6 лет – 0,75 мл;
- до 10 лет – 1,5 мл;
- от 10 лет и взрослым – 3 мл.
Профилактика и лечение гриппа:
- детям до 2 лет – 1,5 мл;
- от 2 до 7 лет – 3 мл;
- от 7 лет и взрослым – 4,5-6 мл.
- однократно с 3-х месяцев, не болевшим и не привитым;
- не позднее 6 суток после контакта с больным;
- дозировка 1,5 — 3 мл.
- однократно с интервалом 24 ч по 3 мл детям, не болевшим и не привитым;
- не позже 3 суток после контакта с больным;
- дозировка 1,5 — 3 мл.
- однократно 3-6 мл непривитым детям и после контакта с больным.
Категорически запрещено вводить препарат внутривенно. Он вводится только по показаниям врача, не применяется вместе с глюконатом кальция.
Введение препарата регистрируют в специальных формах для учета, где указывается номер серии, дата, срок годности и название компании-изготовителя, доза и характер реакции.
Противопоказания к применению

Перед назначением врач обязательно проверят пациента на наличие различных заболеваний, которые могут проявиться при введении белка плазмы:
- аллергические реакции;
- системные иммунопатологические заболевания крови;
- нефрит.
После введения во избежание реакции на лекарство иммуноглобулина, нужно принять любой антигистаминный препарат, и продолжать прием 2-3 дня. Это поможет исключить проявление аллергии. Если у пациента есть уже установленные врачом различные иммунопатологическими заболевания, в таком случае препарат вводят на фоне соответствующей терапии. Взаимодействие его с другими препаратами пока не изучен и нет данных и несовместимости.
Особые указания
Препараты на основе гаммаглобулина человека применяют только по назначению врача. После введения лекарства прививки от кори и паротита проводят не ранее, чем через 3 месяца. Также после вакцинации его вводят не ранее, чем через 2 недели, а в случаях необходимости применения препарата ранее этого срока вакцинацию повторяют. Все другие прививки можно делать в любые сроки, не зависимо от даты введения сыворотки.
Побочные действия

За более чем 25-ти летнюю историю применения препарата врачи сделали тысячи инъекций и этого количества достаточно для того, чтобы получить объективную оценку по его воздействию на организм человека. За это время не были зафиксированы аллергические реакции и развитие анафилактического шока. Поэтому указания на опасность аллергии в инструкции к препарату носит сугубо информативный характер и действительности не соответствует.
Причиной отсутствия аллергии после применения гамма-глобулинов является одинаковая структура константных фрагментов иммуноглобулинов у разных людей и наличие антидиотипической сети – системы антител против антител. Поэтому препараты успешно используют для лечения аллергии.
Антитела класса G в составе препарата блокируют вещества, которые вызывают атопические реакции, поэтому помогают в лечении аллергии и дерматита.
Миф о том, что в результате введения препаратов гамма-глобулинов человека можно заразиться микроорганизмами, не имеет подтверждения. Он возник из-за незнания особенностей состава лекарства, которое не содержит посторонних компонентов. При выделении иммуно-глобулинов из сыворотки задействуют процессы, что на 100% снижают попадание вирусных частиц.
Читайте также 
Сроки, условия хранения и цена

Перед покупкой препарата необходимо тщательно проверить целостность упаковки и сроки. В аптечных условиях его хранят в холодильнике, при температуре 5°С. Отпуск производится строго по рецепту, в свободной продаже лекарство не доступно для покупателей.
Общие требования к хранению препарата:
- температура от 2 до 8°С;
- замораживание не допускается;
- после истечения срока давности подлежит утилизации.
Цена препарата в среднем составляет около 2800-3000 рублей за упаковку №10.
При введении лекарств на основе иммуноглобулина человека необходимо строго придерживаться всех правил, описанных в инструкции. Правильно рассчитанная дозировка, своевременное обращение к врачу и правильное диагностирование – три важных шага на пути преодоления болезни. С каждым годом появляются все более усовершенствованные препараты, которые еще эффективнее помогают в лечении.
 26-07-2019
26-07-2019 0 Просмотров
0 Просмотров 0 комментариев
0 комментариев 0 Рейтинг
0 Рейтинг